Advanced Hybrid Automated Insulin Delivery System based on Successive Linearization Model Predictive Control: The UniBE System
作者: Vihangkumar V. Naik, Eleonora Manzoni, Clara Escorihuela-Altaba, Jose Garcia-Tirado
分类: eess.SY
发布日期: 2025-12-05
备注: 12 pages, 3 Figures, and 5 Tables
💡 一句话要点
提出基于逐次线性化模型预测控制的混合式自动胰岛素输送系统UniBE,提升T1D患者血糖控制。
🎯 匹配领域: 支柱一:机器人控制 (Robot Control)
关键词: 混合式自动胰岛素输送 模型预测控制 逐次线性化 I型糖尿病 血糖控制
📋 核心要点
- 现有hAID系统依赖线性或线性化模型,预测精度受限,影响控制器的决策。
- UniBE系统采用逐次线性化MPC,动态适应血糖变化,减少用户负担。
- 在模拟实验中,UniBE在多种扰动下均表现出良好的血糖控制和低血糖风险。
📝 摘要(中文)
本研究介绍了一种基于逐次线性化模型预测控制(MPC)的混合式自动胰岛素输送(hAID)系统,名为UniBE。该系统集成了基础胰岛素输注和餐后及校正胰岛素追加剂量模块,能够根据血糖动态实时调整边界,并考虑自动和用户发起的输入。通过FDA批准的UVa/Padova代谢模拟器的商业版本,在九种场景下进行了计算机模拟评估,这些场景涉及餐食时间、碳水化合物估计和基础胰岛素曲线中的持续和时变误差。在基线场景中,UniBE的平均血糖目标范围内时间为92.0+-13.2%,低于目标范围的时间为0.1+-0.2%,高于目标范围的时间为7.9+-13.2%。在扰动场景中,血糖目标范围内时间保持在75.1%到92.8%之间,低血糖发生率较低,表明其对临床相关干扰具有弹性。
🔬 方法详解
问题定义:当前混合式自动胰岛素输送系统依赖于线性或线性化模型来预测血糖变化,这在生理变异性较大和存在各种干扰因素(如餐食时间不确定、碳水化合物估计误差等)的情况下,会降低预测精度,从而影响胰岛素输送的决策质量。因此,需要一种能够更准确预测血糖变化,并能适应个体差异和各种干扰的控制系统。
核心思路:UniBE系统的核心思路是采用逐次线性化模型预测控制(MPC)。通过在每个控制周期内对非线性血糖动态模型进行线性化,可以更准确地预测短时间内的血糖变化。同时,MPC能够根据预测结果优化胰岛素输送策略,并在满足安全约束(如避免低血糖)的前提下,尽可能地将血糖维持在目标范围内。
技术框架:UniBE系统主要包含以下几个模块:1) 血糖传感器:实时监测血糖水平;2) 逐次线性化模型预测控制器:基于血糖动态模型,预测未来一段时间内的血糖变化,并优化胰岛素输送策略;3) 胰岛素泵:根据控制器的指令,输送基础胰岛素和追加胰岛素;4) 用户界面:允许用户输入餐食信息、进行校正剂量等操作。整个系统通过闭环控制,不断调整胰岛素输送,以维持血糖稳定。
关键创新:UniBE系统的关键创新在于采用了逐次线性化模型预测控制。与传统的线性或线性化模型相比,逐次线性化能够更准确地捕捉非线性血糖动态,从而提高预测精度和控制性能。此外,该系统还能够根据血糖动态实时调整控制器的边界,进一步提高其适应性和鲁棒性。
关键设计:UniBE系统采用的血糖动态模型是UVa/Padova代谢模拟器中的模型。控制器采用模型预测控制,目标函数包括血糖与目标值的偏差、胰岛素输送量的变化等。约束条件包括血糖上下限、胰岛素输送速率上下限等。逐次线性化通过在每个控制周期内计算血糖动态模型在当前状态下的雅可比矩阵来实现。
🖼️ 关键图片
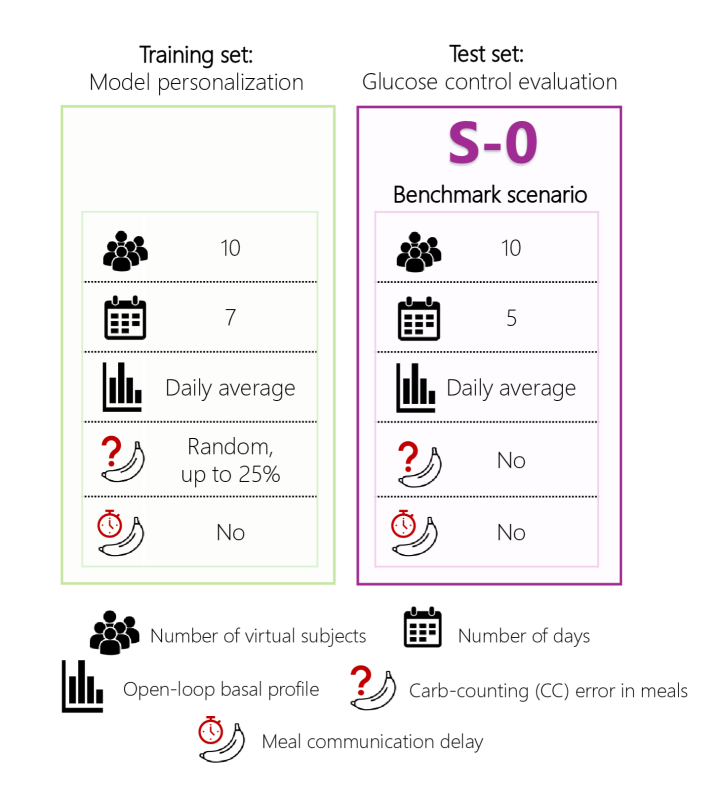

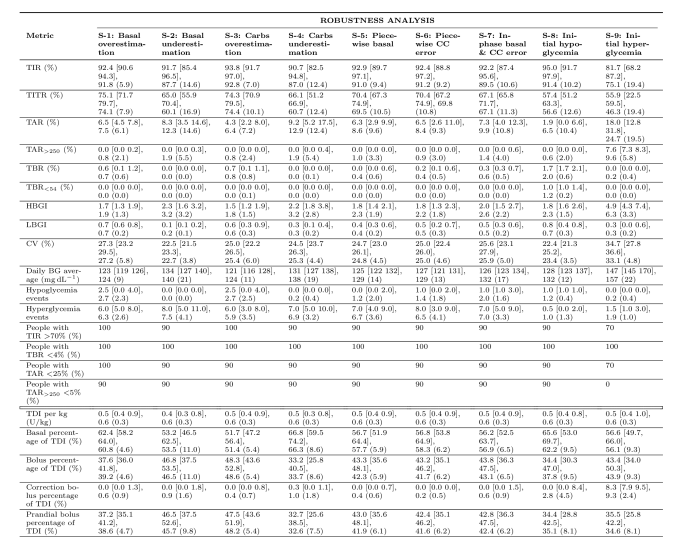
📊 实验亮点
UniBE系统在模拟实验中表现出色。在基线场景下,血糖目标范围内时间达到92.0%,低血糖发生率仅为0.1%。在餐食时间、碳水化合物估计和基础胰岛素曲线存在误差的扰动场景下,血糖目标范围内时间仍保持在75.1%到92.8%之间,表明该系统具有良好的鲁棒性和抗干扰能力。这些结果表明UniBE系统具有显著的临床应用潜力。
🎯 应用场景
UniBE系统可应用于I型糖尿病患者的血糖管理,通过自动调整胰岛素输送,减轻患者负担,提高生活质量。该系统具有良好的适应性和鲁棒性,能够应对餐食不确定、碳水化合物估计误差等实际临床场景中的干扰。未来,该系统有望进一步集成连续血糖监测(CGM)和人工智能技术,实现更个性化、更智能的血糖控制。
📄 摘要(原文)
Background and objective: Hybrid automated insulin delivery (hAID) systems represent the most advanced therapy for type 1 diabetes (T1D). Current systems rely on linear or linearized models of glucose homeostasis, which may compromise prediction accuracy and, in turn, timely decision-making by the controller. Physiological variability further complicates insulin requirements, underscoring the need for controllers that adapt dynamically and reduce user burden. Methods: We introduce the University of Bern (UniBE) hAID system, a framework based on successive linearization model predictive control (MPC). The controller integrates basal insulin infusion with the insulin bolus delivery module for meal-related and corrective bolus dosing, adapting bounds in real time to glucose dynamics while accounting for both automated and user-initiated inputs. In-silico evaluation was conducted using the commercial version of the FDA-accepted UVa/Padova metabolic simulator across nine scenarios involving persistent and time-varying errors in meal timing, carbohydrate estimation, and basal insulin profiles. Results: In the baseline scenario, UniBE achieved a mean time in range of 92.0+-13.2%, with time below range at 0.1+-0.2% and time above range at 7.9+-13.2%. Across perturbation scenarios, time in range remained between 75.1 and 92.8%, with low hypoglycemia incidence, demonstrating resilience to clinically relevant disturbances.