Towards Applying Large Language Models to Complement Single-Cell Foundation Models
作者: Steven Palayew, Bo Wang, Gary Bader
分类: cs.LG, q-bio.GN
发布日期: 2025-07-14
💡 一句话要点
提出scMPT模型,融合单细胞Foundation模型与LLM,提升单细胞分析性能。
🎯 匹配领域: 支柱九:具身大模型 (Embodied Foundation Models)
关键词: 单细胞分析 Foundation模型 大型语言模型 多模态融合 scGPT 细胞类型识别 生物信息学
📋 核心要点
- 单细胞Foundation模型无法有效利用生物学领域中大量的文本信息,限制了其性能。
- 论文提出scMPT模型,通过融合scGPT和LLM的单细胞表示,捕捉生物学见解,实现优势互补。
- 实验结果表明,scMPT模型比单独使用scGPT或LLM表现更强、更稳定,验证了融合方法的有效性。
📝 摘要(中文)
单细胞Foundation模型,如scGPT,在单细胞组学领域取得了显著进展,并在各种下游生物任务中表现出最先进的性能。然而,这些模型本质上存在局限性,即生物学中大量信息以文本形式存在,而它们无法利用这些信息。因此,最近的一些工作提出了使用LLM作为单细胞Foundation模型的替代方案,并取得了具有竞争力的结果。然而,人们对驱动这种性能的因素知之甚少,并且非常关注将LLM作为一种替代方案,而不是作为单细胞Foundation模型的补充方法。在本研究中,我们因此研究了当LLM应用于单细胞数据时,哪些生物学见解有助于其性能,并介绍了scMPT;该模型利用了scGPT和来自LLM的单细胞表示之间的协同作用,这些表示捕获了这些见解。scMPT表现出比其任何一个组成模型更强大、更一致的性能,而这些模型之间在数据集上的性能经常存在很大差距。我们还尝试了替代融合方法,展示了将专门的推理模型与scGPT相结合以提高性能的潜力。这项研究最终展示了LLM补充单细胞Foundation模型并推动单细胞分析改进的潜力。
🔬 方法详解
问题定义:现有单细胞Foundation模型,如scGPT,虽然在处理单细胞组学数据方面表现出色,但无法有效利用生物学领域中以文本形式存在的大量知识。这限制了模型对复杂生物学问题的理解和解决能力。同时,直接使用LLM作为替代方案,缺乏对驱动其性能的生物学因素的深入理解。
核心思路:论文的核心思路是将单细胞Foundation模型(scGPT)与LLM的优势结合起来,构建一个互补的模型scMPT。通过融合两种模型的单细胞表示,scMPT能够同时利用组学数据和文本知识,从而更全面地理解单细胞的生物学特性。这种融合方法旨在克服单一模型的局限性,提高单细胞分析的性能。
技术框架:scMPT模型的整体框架包括两个主要组成部分:scGPT和LLM。首先,使用scGPT处理单细胞组学数据,提取细胞的特征表示。然后,使用LLM处理相关的生物学文本信息,生成文本相关的细胞表示。最后,通过融合模块将两种表示进行融合,得到最终的单细胞表示,用于下游任务,如细胞类型分类、细胞状态预测等。论文还尝试了不同的融合方法,探索最佳的融合策略。
关键创新:论文的关键创新在于提出了一个将单细胞Foundation模型与LLM相结合的互补框架。与以往研究中将LLM作为单细胞Foundation模型的替代方案不同,该研究强调了两种模型的协同作用,通过融合两种模型的表示,实现了性能的提升。此外,论文还深入研究了驱动LLM在单细胞数据上表现的生物学因素,为模型的设计提供了理论依据。
关键设计:论文实验了多种融合方法,包括简单的拼接、加权平均等。具体参数设置和网络结构细节在论文中未详细说明,属于未知信息。损失函数的设计也未明确提及,可能使用了标准的分类或回归损失函数,具体取决于下游任务。
🖼️ 关键图片

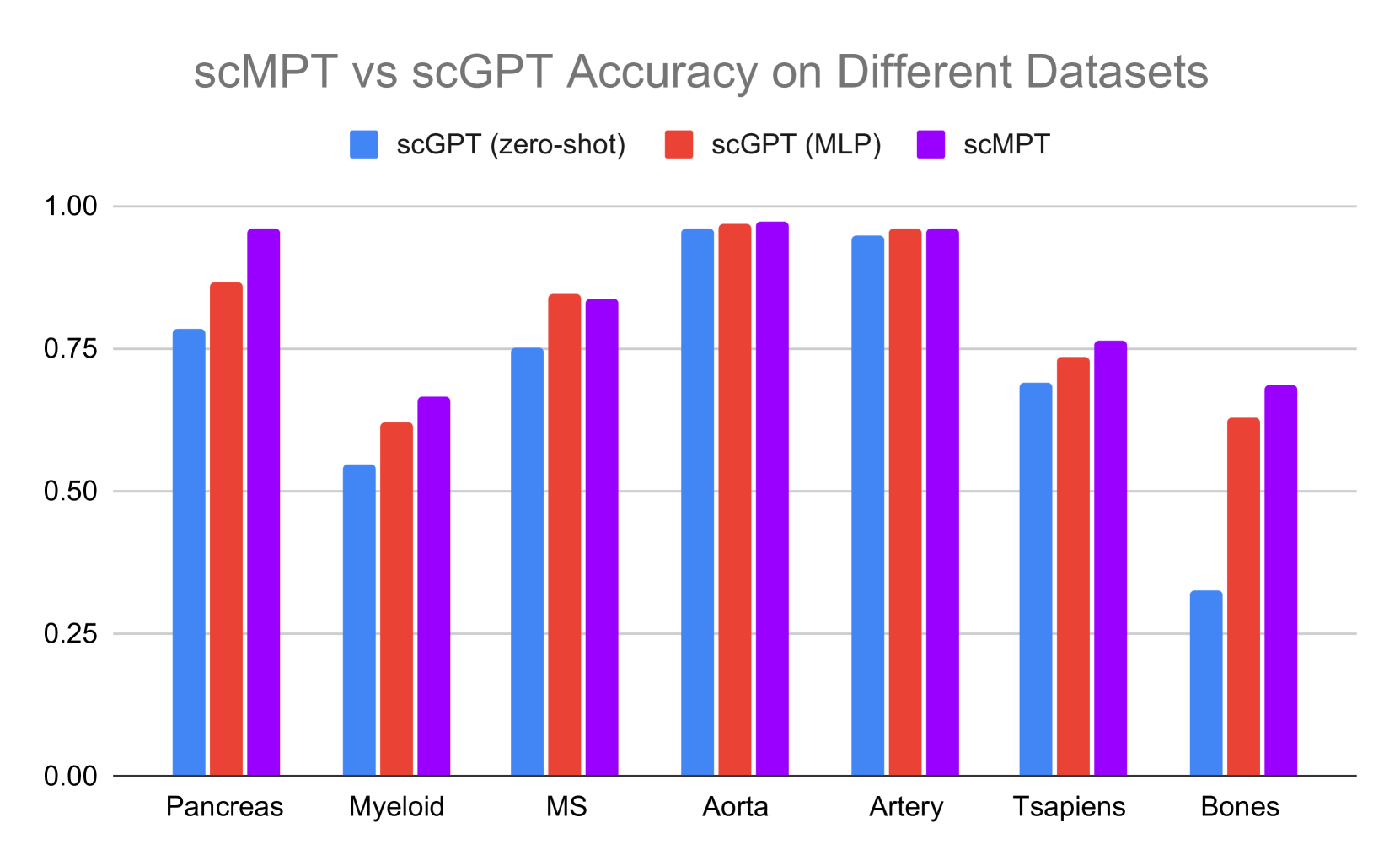
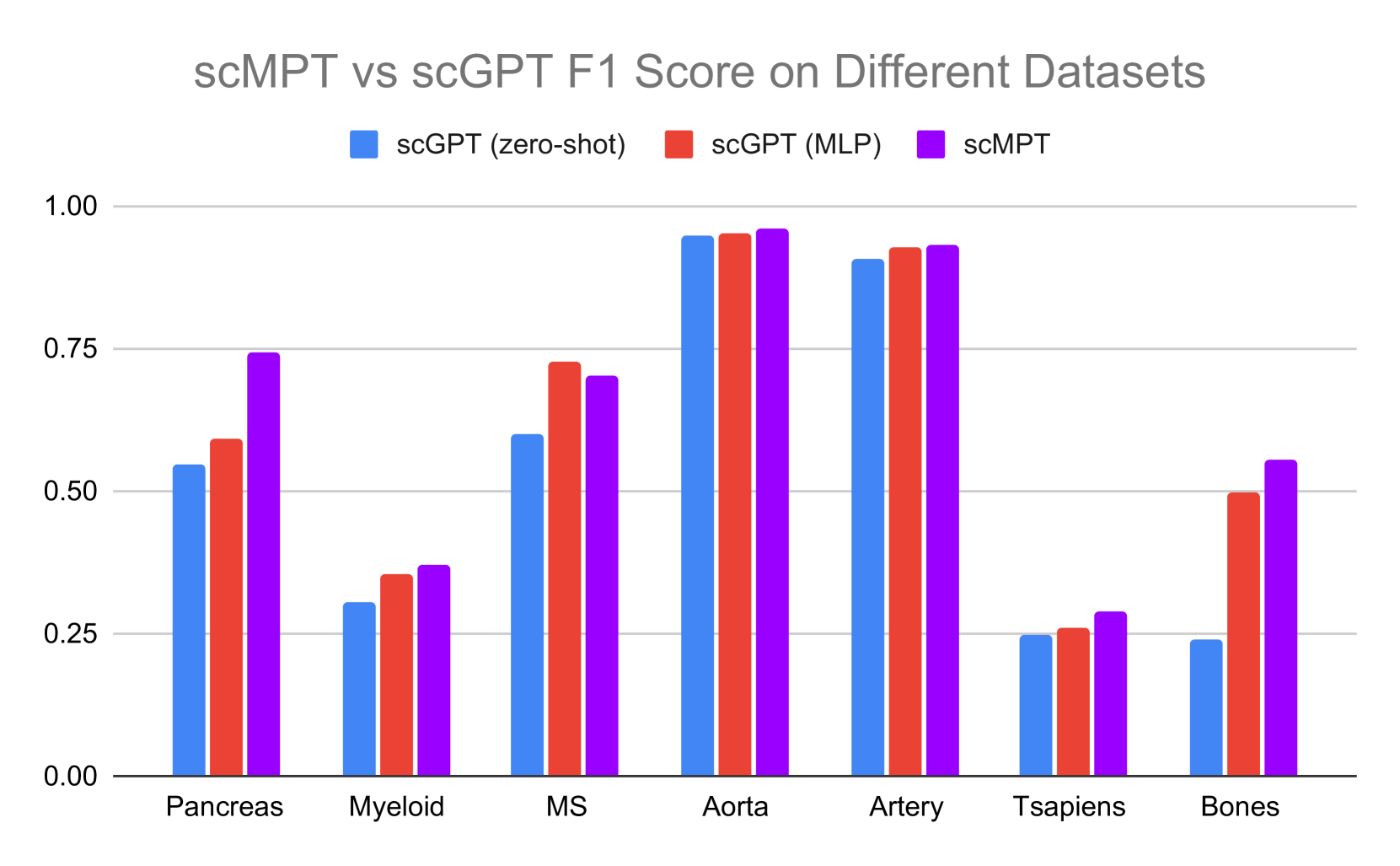
📊 实验亮点
scMPT模型在多个单细胞数据集上表现出比单独使用scGPT或LLM更强大、更稳定的性能。具体性能提升幅度因数据集而异,但总体趋势是scMPT能够克服单一模型的局限性,实现更好的泛化能力。此外,论文还探索了不同的融合方法,并展示了将专门的推理模型与scGPT相结合以提高性能的潜力。
🎯 应用场景
该研究成果可应用于单细胞生物学的多个领域,例如细胞类型识别、细胞状态预测、疾病机制研究和药物发现。通过结合组学数据和文本知识,可以更准确地理解细胞的生物学特性,从而为疾病诊断和治疗提供新的思路。未来,该方法有望应用于更复杂的生物学问题,例如多组学数据整合和个性化医疗。
📄 摘要(原文)
Single-cell foundation models such as scGPT represent a significant advancement in single-cell omics, with an ability to achieve state-of-the-art performance on various downstream biological tasks. However, these models are inherently limited in that a vast amount of information in biology exists as text, which they are unable to leverage. There have therefore been several recent works that propose the use of LLMs as an alternative to single-cell foundation models, achieving competitive results. However, there is little understanding of what factors drive this performance, along with a strong focus on using LLMs as an alternative, rather than complementary approach to single-cell foundation models. In this study, we therefore investigate what biological insights contribute toward the performance of LLMs when applied to single-cell data, and introduce scMPT; a model which leverages synergies between scGPT, and single-cell representations from LLMs that capture these insights. scMPT demonstrates stronger, more consistent performance than either of its component models, which frequently have large performance gaps between each other across datasets. We also experiment with alternate fusion methods, demonstrating the potential of combining specialized reasoning models with scGPT to improve performance. This study ultimately showcases the potential for LLMs to complement single-cell foundation models and drive improvements in single-cell analysis.