OmegAMP: Targeted AMP Discovery through Biologically Informed Generation
作者: Diogo Soares, Leon Hetzel, Paulina Szymczak, Marcelo Der Torossian Torres, Johanna Sommer, Cesar de la Fuente-Nunez, Fabian Theis, Stephan Günnemann, Ewa Szczurek
分类: cs.LG, cs.AI, q-bio.BM
发布日期: 2025-04-24 (更新: 2025-10-29)
💡 一句话要点
OmegAMP:通过生物信息指导的生成方法实现靶向抗菌肽发现
🎯 匹配领域: 支柱八:物理动画 (Physics-based Animation)
关键词: 抗菌肽发现 深度学习 扩散模型 生物信息学 生成模型 药物设计 抗生素耐药性
📋 核心要点
- 现有基于深度学习的抗菌肽发现方法,在可控性、抗菌特性建模和实验命中率方面存在不足。
- OmegAMP利用扩散模型和生物信息编码空间,实现对抗菌肽理化性质和活性谱的细粒度控制。
- 实验结果表明,OmegAMP显著提高了抗菌肽发现的成功率,对多重耐药菌株也有效,具有实际应用价值。
📝 摘要(中文)
基于深度学习的抗菌肽(AMP)发现面临着可控性有限、缺乏有效建模抗菌特性的表征以及实验命中率低等关键挑战。为了解决这些问题,我们提出了OmegAMP,一个旨在实现可靠AMP生成并提高可控性的框架。其基于扩散的生成模型利用了一种新颖的调节机制,以实现对所需理化性质的细粒度控制,并将生成导向特定的活性谱,包括物种特异性有效性。生物信息编码空间进一步增强了这一点,显著提高了整体生成性能。作为这些生成能力的补充,OmegAMP利用一种新颖的合成数据增强策略来训练AMP过滤分类器,从而大幅降低了假阳性率,并提高了实验成功的可能性。我们的计算机模拟实验表明,OmegAMP在AMP发现流程的关键阶段提供了最先进的性能,使我们能够在湿实验室实验中取得前所未有的成功率。我们测试了25个候选肽,其中24个(96%)表现出抗菌活性,甚至对多重耐药菌株也有效。我们的发现强调了OmegAMP在对抗抗菌素耐药性方面显著推进计算框架的潜力。
🔬 方法详解
问题定义:现有基于深度学习的抗菌肽发现方法存在三个主要痛点:一是生成过程缺乏可控性,难以根据需求定制抗菌肽;二是缺乏能够有效建模抗菌特性的表征方法;三是实验验证的命中率较低,导致研发成本高昂。
核心思路:OmegAMP的核心思路是利用生物信息指导的扩散模型,实现对抗菌肽生成过程的精确控制。通过结合理化性质和活性谱等生物信息,引导模型生成具有特定功能的抗菌肽。同时,采用合成数据增强策略,提高分类器的性能,降低假阳性率。
技术框架:OmegAMP框架主要包含三个模块:1) 基于扩散模型的抗菌肽生成器,利用生物信息进行条件控制;2) 生物信息编码空间,用于高效建模抗菌肽的性质;3) 基于合成数据增强的抗菌肽过滤器,用于降低假阳性率。整体流程为:首先,利用生成器生成候选抗菌肽;然后,利用过滤器筛选出具有潜在活性的抗菌肽;最后,进行实验验证。
关键创新:OmegAMP的关键创新在于:1) 提出了基于扩散模型的抗菌肽生成方法,实现了对生成过程的细粒度控制;2) 设计了生物信息编码空间,能够有效建模抗菌肽的性质;3) 采用了合成数据增强策略,提高了分类器的性能。与现有方法相比,OmegAMP能够更高效地生成具有特定功能的抗菌肽,并显著提高实验验证的成功率。
关键设计:在扩散模型中,作者使用了一种新颖的调节机制,允许用户指定抗菌肽的理化性质和活性谱。生物信息编码空间的设计考虑了抗菌肽的氨基酸序列、结构和功能等因素。合成数据增强策略通过生成具有不同性质的抗菌肽,扩充了训练数据集,提高了分类器的泛化能力。损失函数的设计旨在平衡生成质量和活性预测的准确性。
🖼️ 关键图片

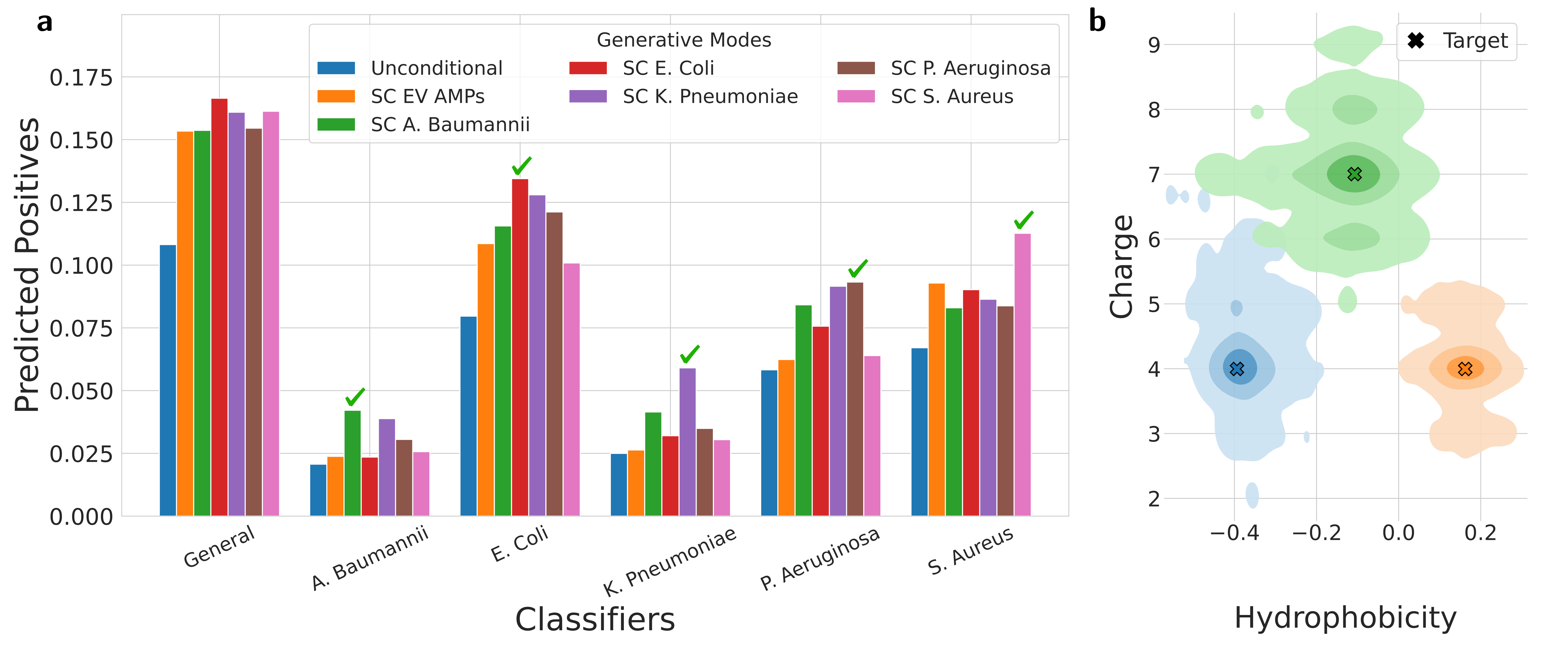
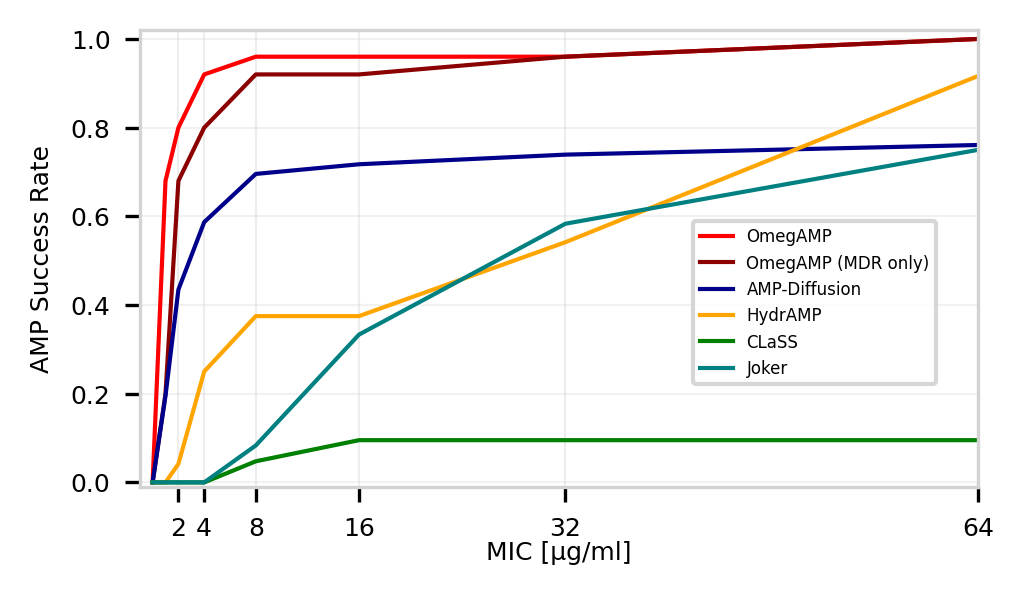
📊 实验亮点
OmegAMP在体外实验中取得了显著的成果,对25个候选肽进行了测试,其中24个(96%)表现出抗菌活性,即使对多重耐药菌株也有效。这一成功率远高于传统方法,证明了OmegAMP在抗菌肽发现方面的优越性。该研究表明,通过结合深度学习和生物信息学,可以显著提高药物发现的效率。
🎯 应用场景
OmegAMP在抗菌肽药物发现领域具有广阔的应用前景,可用于开发新型抗菌药物,应对日益严重的抗生素耐药性问题。该框架还可以应用于其他生物活性肽的发现,例如抗肿瘤肽和免疫调节肽等。此外,OmegAMP的生物信息指导生成方法,为其他生物分子设计提供了新的思路。
📄 摘要(原文)
Deep learning-based antimicrobial peptide (AMP) discovery faces critical challenges such as limited controllability, lack of representations that efficiently model antimicrobial properties, and low experimental hit rates. To address these challenges, we introduce OmegAMP, a framework designed for reliable AMP generation with increased controllability. Its diffusion-based generative model leverages a novel conditioning mechanism to achieve fine-grained control over desired physicochemical properties and to direct generation towards specific activity profiles, including species-specific effectiveness. This is further enhanced by a biologically informed encoding space that significantly improves overall generative performance. Complementing these generative capabilities, OmegAMP leverages a novel synthetic data augmentation strategy to train classifiers for AMP filtering, drastically reducing false positive rates and thereby increasing the likelihood of experimental success. Our in silico experiments demonstrate that OmegAMP delivers state-of-the-art performance across key stages of the AMP discovery pipeline, enabling us to achieve an unprecedented success rate in wet lab experiments. We tested 25 candidate peptides, 24 of them (96%) demonstrated antimicrobial activity, proving effective even against multi-drug resistant strains. Our findings underscore OmegAMP's potential to significantly advance computational frameworks in the fight against antimicrobial resistance.