GUIDE-US: Grade-Informed Unpaired Distillation of Encoder Knowledge from Histopathology to Micro-UltraSound
作者: Emma Willis, Tarek Elghareb, Paul F. R. Wilson, Minh Nguyen Nhat To, Mohammad Mahdi Abootorabi, Amoon Jamzad, Brian Wodlinger, Parvin Mousavi, Purang Abolmaesumi
分类: cs.CV, cs.LG
发布日期: 2026-02-22
备注: Accepted to IPCAI 2026
💡 一句话要点
提出GUIDE-US,利用非配对组织病理学知识蒸馏提升微超声前列腺癌分级性能。
🎯 匹配领域: 支柱二:RL算法与架构 (RL & Architecture) 支柱九:具身大模型 (Embodied Foundation Models)
关键词: 前列腺癌分级 微超声 知识蒸馏 非配对学习 组织病理学 医学图像分析 深度学习
📋 核心要点
- 现有微超声前列腺癌分级模型难以在高分辨率下推断组织微结构,限制了临床应用。
- 提出一种非配对知识蒸馏方法,利用组织病理学知识指导微超声编码器的训练,无需图像配准。
- 实验表明,该方法显著提高了临床显著性前列腺癌的检测敏感性,提升了早期风险分层的能力。
📝 摘要(中文)
本研究旨在利用微超声(micro-US)对前列腺癌(PCa)进行无创分级,以加速分诊并引导活检至最具侵袭性的区域。然而,现有模型难以在粗糙的成像分辨率下推断组织微结构。为此,我们提出了一种非配对的组织病理学知识蒸馏策略,该策略训练微超声编码器来模拟预训练的组织病理学基础模型的嵌入分布,并以国际泌尿病理学会(ISUP)等级为条件。训练不需要患者级别的配对或图像配准,并且在推理时不使用组织病理学输入。实验结果表明,与当前最先进的方法相比,我们的方法在60%特异性下,对临床显著性PCa(csPCa)的敏感性提高了3.5%,并且在60%特异性下,总体敏感性提高了1.2%。通过仅从成像实现更早和更可靠的癌症风险分层,我们的方法提高了临床可行性。源代码将在发表后公开发布。
🔬 方法详解
问题定义:现有方法在利用微超声进行前列腺癌分级时,由于微超声图像分辨率较低,难以准确推断组织微结构,导致分级精度不足,影响临床决策。现有方法依赖于有监督学习,需要配对的微超声和组织病理学图像,数据获取成本高昂。
核心思路:利用知识蒸馏的思想,将预训练的组织病理学基础模型中的知识迁移到微超声编码器中。组织病理学图像包含更丰富的组织微结构信息,可以作为微超声编码器的学习目标。通过非配对的方式进行知识蒸馏,避免了对配对数据的依赖,降低了数据获取成本。
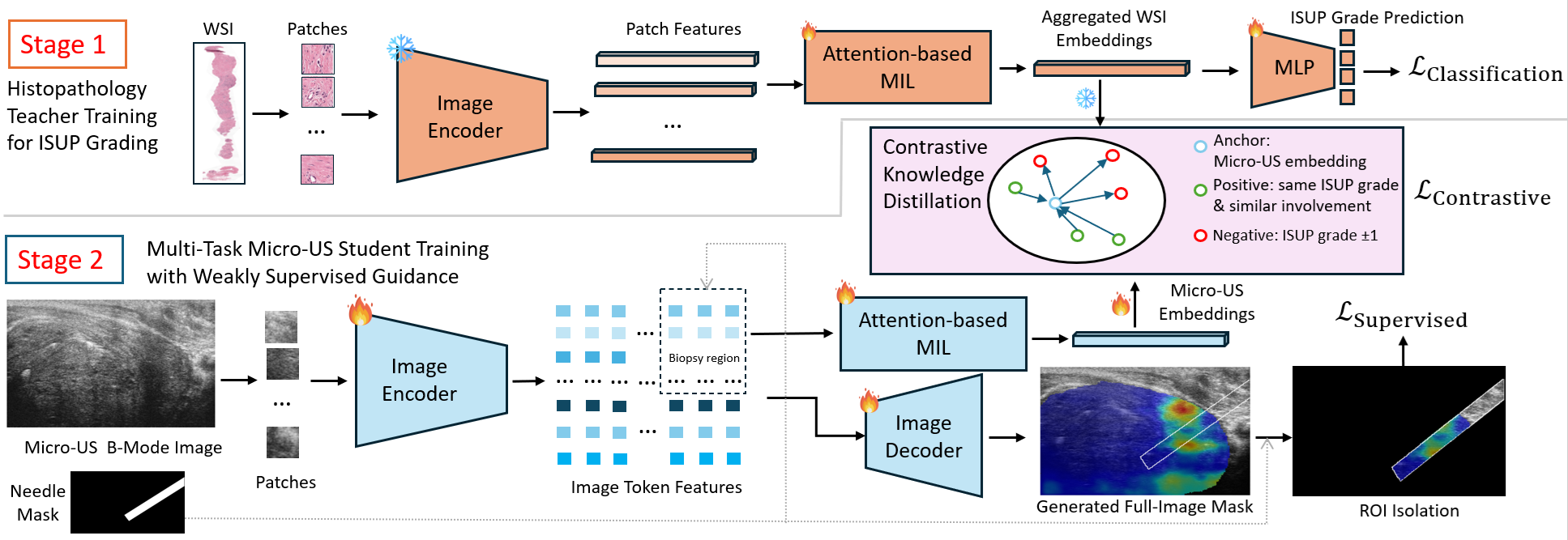
技术框架:该方法包含两个主要模块:预训练的组织病理学编码器和待训练的微超声编码器。首先,使用大量组织病理学图像预训练一个编码器,使其能够提取组织微结构的特征表示。然后,使用非配对的微超声和组织病理学图像,训练微超声编码器,使其输出的特征表示与组织病理学编码器的输出分布尽可能接近。训练过程中,使用ISUP等级作为条件,引导微超声编码器学习不同等级前列腺癌的特征表示。
关键创新:该方法的核心创新在于使用非配对的知识蒸馏方法,将组织病理学知识迁移到微超声编码器中。与传统的知识蒸馏方法不同,该方法不需要配对的图像数据,降低了数据获取成本。此外,该方法使用ISUP等级作为条件,引导微超声编码器学习不同等级前列腺癌的特征表示,提高了分级精度。
关键设计:组织病理学编码器采用预训练的深度学习模型,例如ResNet或Transformer。微超声编码器采用类似的结构,但参数量较小。损失函数包括两部分:一部分是用于衡量微超声编码器输出的特征表示与组织病理学编码器输出分布之间差异的距离损失,例如KL散度或MMD距离;另一部分是用于衡量微超声编码器输出的特征表示与ISUP等级之间一致性的分类损失。
🖼️ 关键图片
📊 实验亮点
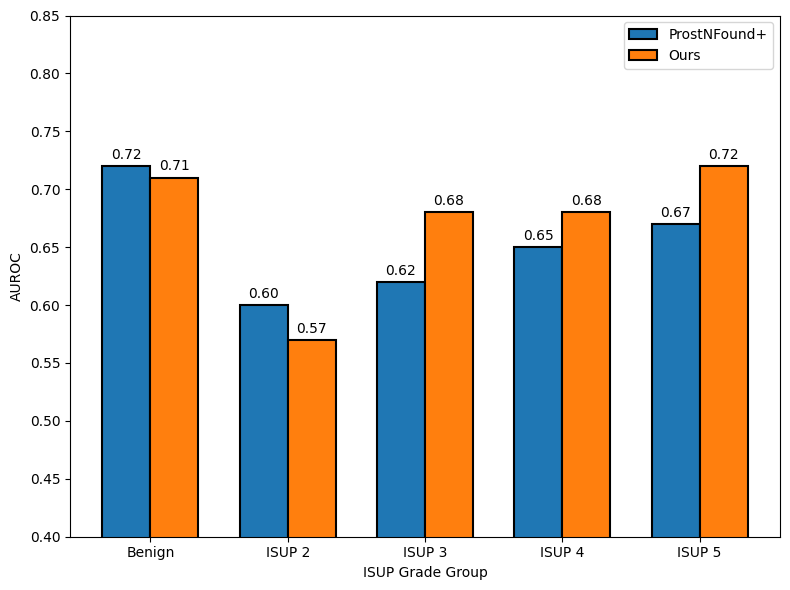
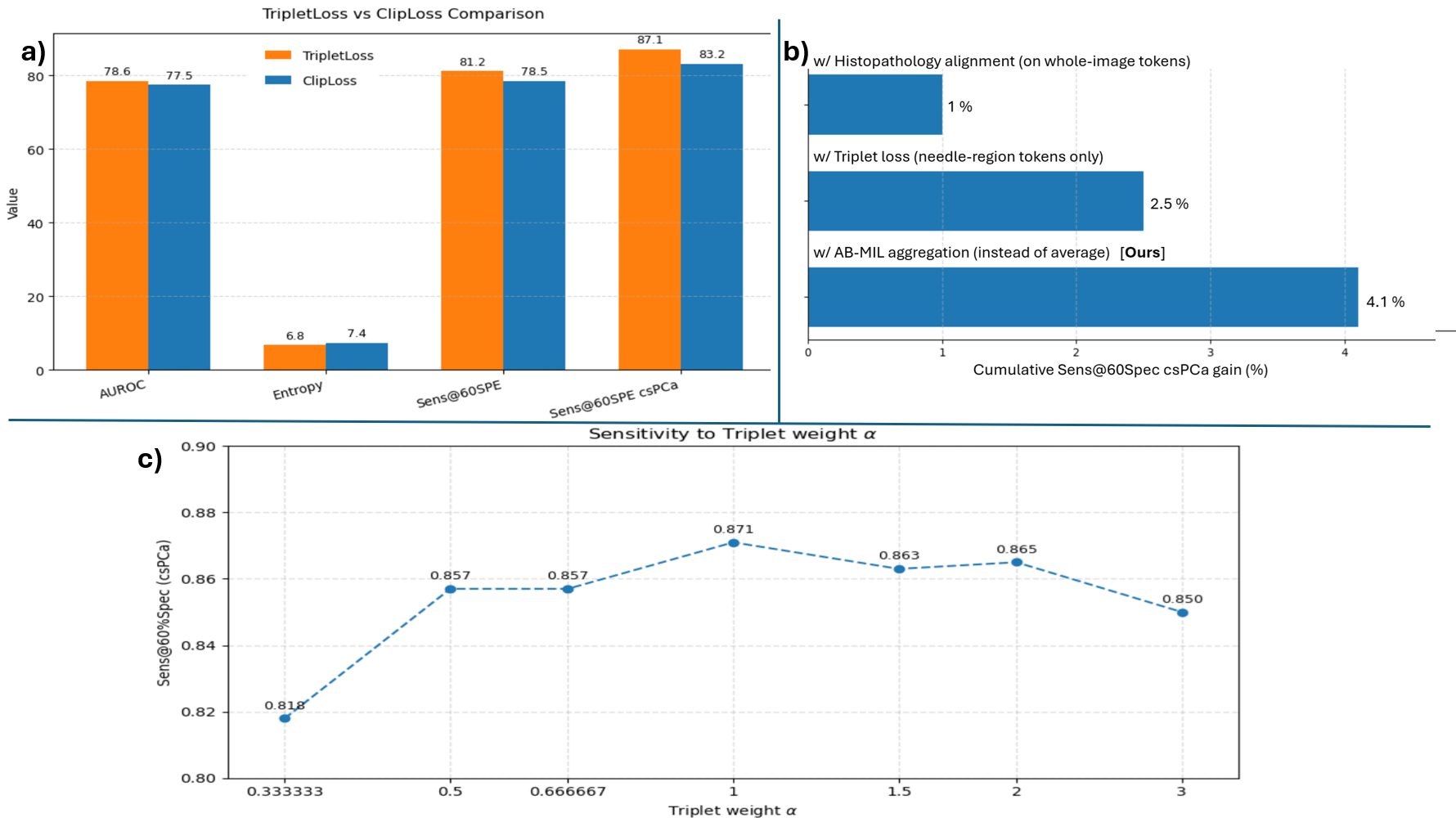
实验结果表明,与当前最先进的方法相比,该方法在60%特异性下,对临床显著性PCa(csPCa)的敏感性提高了3.5%,并且在60%特异性下,总体敏感性提高了1.2%。这表明该方法能够更准确地检测出具有临床意义的前列腺癌,有助于早期诊断和治疗。
🎯 应用场景
该研究成果可应用于前列腺癌的早期筛查和风险分层,通过微超声成像即可实现无创评估,减少不必要的活检。该方法还可推广到其他癌症类型的诊断,提升医疗效率,降低患者痛苦,具有广阔的临床应用前景。
📄 摘要(原文)
Purpose: Non-invasive grading of prostate cancer (PCa) from micro-ultrasound (micro-US) could expedite triage and guide biopsies toward the most aggressive regions, yet current models struggle to infer tissue micro-structure at coarse imaging resolutions. Methods: We introduce an unpaired histopathology knowledge-distillation strategy that trains a micro-US encoder to emulate the embedding distribution of a pretrained histopathology foundation model, conditioned on International Society of Urological Pathology (ISUP) grades. Training requires no patient-level pairing or image registration, and histopathology inputs are not used at inference. Results: Compared to the current state of the art, our approach increases sensitivity to clinically significant PCa (csPCa) at 60% specificity by 3.5% and improves overall sensitivity at 60% specificity by 1.2%. Conclusion: By enabling earlier and more dependable cancer risk stratification solely from imaging, our method advances clinical feasibility. Source code will be publicly released upon publication.