Self-Supervised Masked Autoencoders with Dense-Unet for Coronary Calcium Removal in limited CT Data
作者: Mo Chen
分类: cs.CV, cs.AI
发布日期: 2025-12-25
备注: 6 pages, in Chinese language, 2 figures
💡 一句话要点
提出Dense-MAE,利用自监督学习去除有限CT数据中的冠状动脉钙化伪影。
🎯 匹配领域: 支柱二:RL算法与架构 (RL & Architecture)
关键词: 自监督学习 掩码自编码器 冠状动脉钙化去除 医学图像处理 Dense-Unet
📋 核心要点
- 冠状动脉钙化伪影影响CTA图像质量,现有DCNN方法依赖大量标注数据,医学领域数据稀缺。
- 提出Dense-MAE,通过掩码血管腔的3D补丁并重建,自监督学习动脉拓扑的高级特征。
- 实验表明,使用Dense-MAE预训练权重初始化网络,显著提升了钙去除的修复精度和狭窄估计。
📝 摘要(中文)
冠状动脉钙化会在计算机断层扫描血管造影(CTA)中产生伪影,严重阻碍管腔狭窄的诊断。深度卷积神经网络(DCNN),如Dense-Unet,已显示出通过图像修复去除这些伪影的潜力,但它们通常需要大量的标记数据集,而这在医学领域是稀缺的。受3D点云掩码自编码器(MAE)最新进展的启发,我们提出Dense-MAE,一种用于体积医学数据的新型自监督学习框架。我们引入了一种预训练策略,随机掩盖血管腔的3D补丁,并训练Dense-Unet来重建缺失的几何形状。这迫使编码器在没有人为注释的情况下学习动脉拓扑的高级潜在特征。在临床CTA数据集上的实验结果表明,与从头开始训练相比,使用基于MAE的权重初始化钙去除网络可以显著提高修复精度和狭窄估计,尤其是在少样本场景中。
🔬 方法详解
问题定义:论文旨在解决计算机断层扫描血管造影(CTA)图像中,由冠状动脉钙化引起的伪影问题。这些伪影会严重影响医生对血管狭窄程度的判断,从而影响诊断。现有的深度学习方法,例如Dense-Unet,虽然可以用于去除这些伪影,但通常需要大量的标注数据进行训练,而在医学图像领域,高质量的标注数据往往非常稀缺,获取成本高昂。
核心思路:论文的核心思路是利用自监督学习的方式,预训练一个能够学习血管拓扑结构高级特征的模型。具体来说,就是通过掩盖CTA图像中的一部分区域,然后让模型去重建这些被掩盖的区域。通过这种方式,模型可以学习到血管的内在结构和几何信息,而无需人工标注。
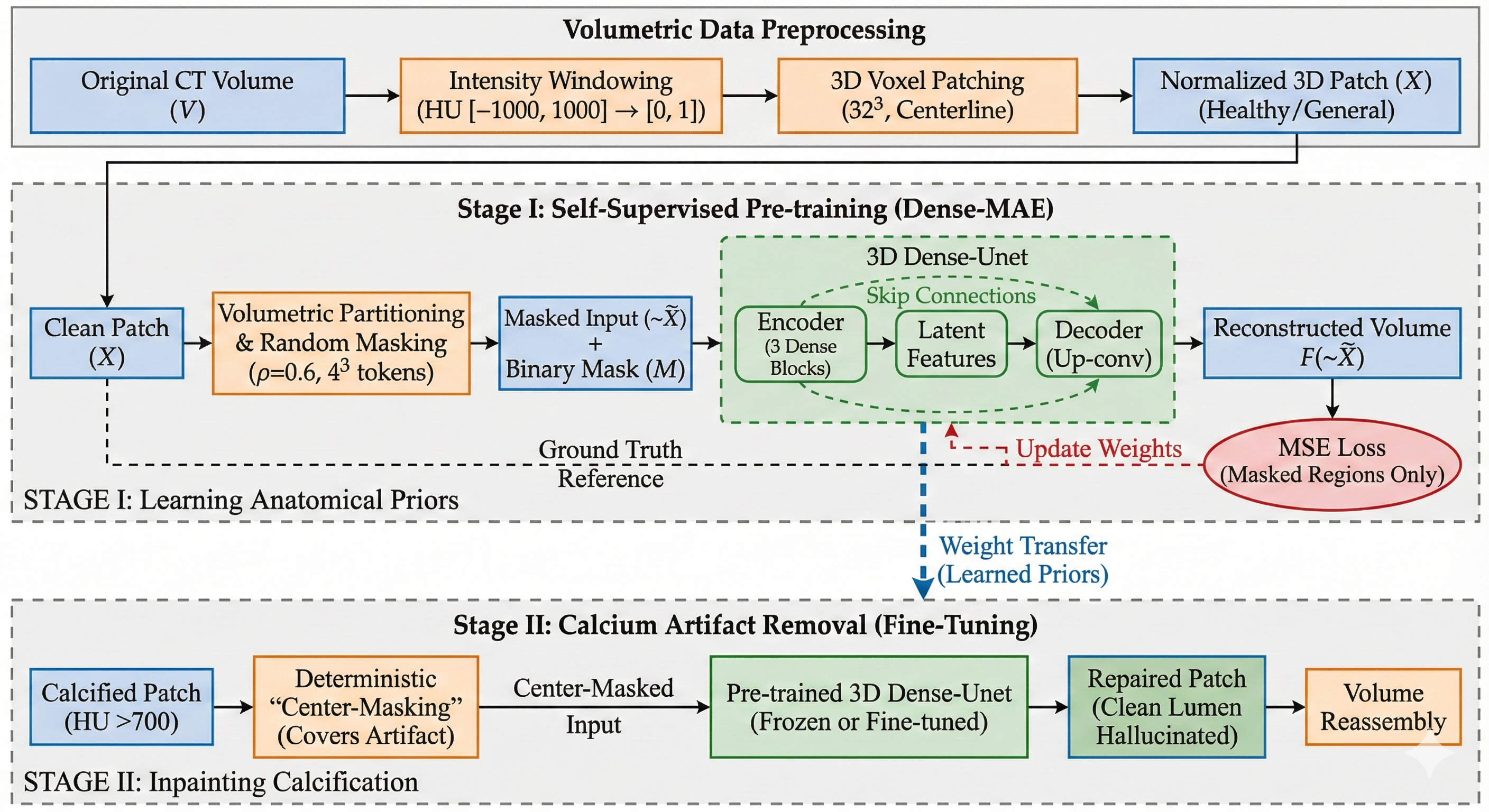
技术框架:Dense-MAE的整体框架基于掩码自编码器(MAE)的思想,并结合了Dense-Unet的网络结构。首先,随机掩盖输入CTA图像中的3D补丁。然后,将掩盖后的图像输入到Dense-Unet编码器中,提取潜在特征。接着,使用Dense-Unet解码器,根据潜在特征重建被掩盖的区域。最后,通过计算重建区域与原始区域之间的损失,来训练模型。
关键创新:论文的关键创新在于将MAE的思想应用到医学图像领域,并结合了Dense-Unet的网络结构,提出了Dense-MAE。与传统的监督学习方法相比,Dense-MAE不需要大量的标注数据,就可以学习到血管拓扑结构的高级特征。此外,通过掩盖3D补丁的方式,可以迫使模型学习到更加鲁棒的特征表示。
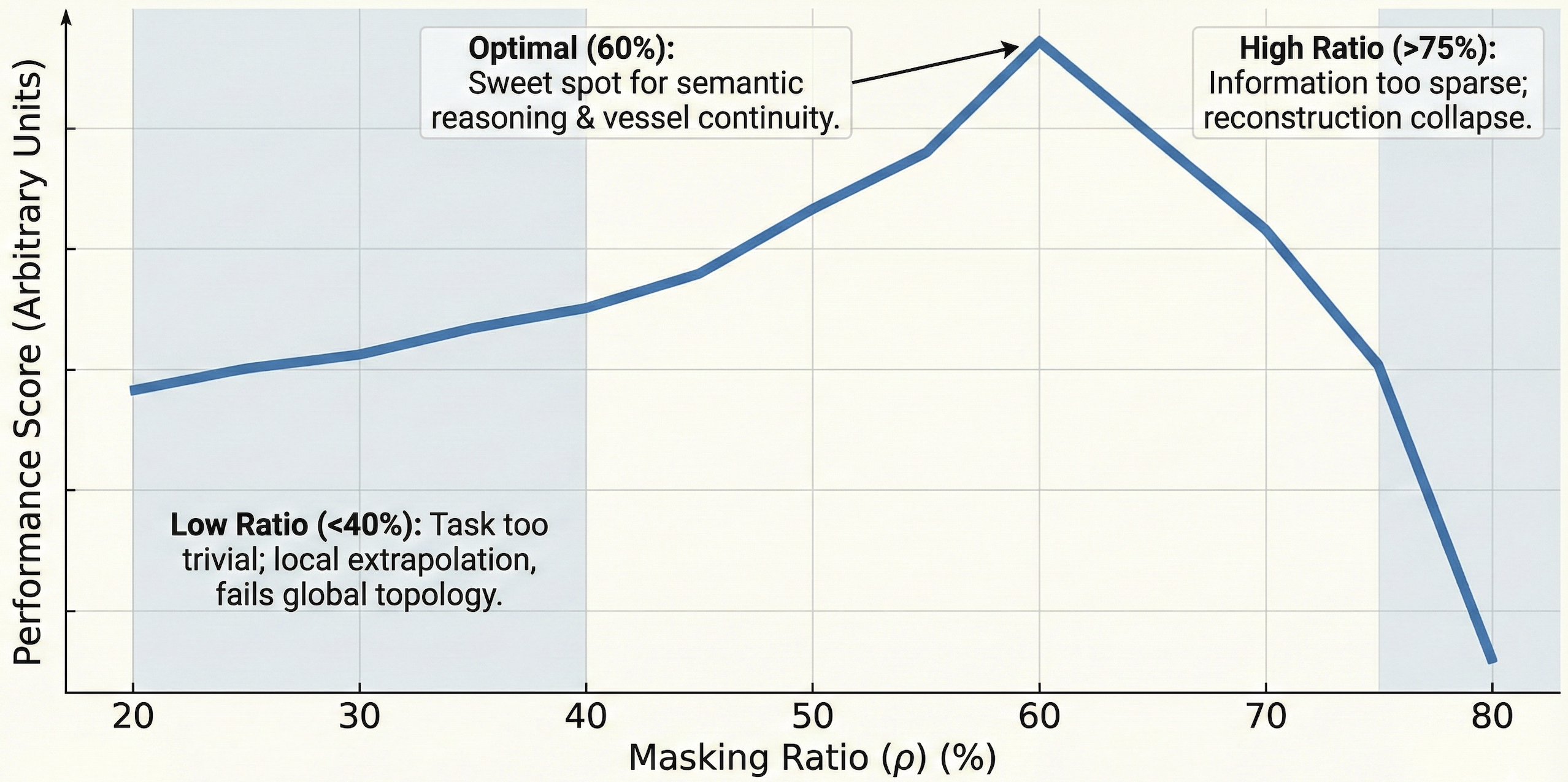
关键设计:论文中,3D补丁的掩盖比例是一个重要的参数。作者通过实验发现,较高的掩盖比例可以迫使模型学习到更加全局的特征。损失函数采用的是均方误差(MSE),用于衡量重建区域与原始区域之间的差异。Dense-Unet的网络结构采用了密集连接的方式,可以有效地利用不同尺度的特征信息。
🖼️ 关键图片
📊 实验亮点
实验结果表明,在有限的CTA数据下,使用Dense-MAE预训练的Dense-Unet模型,在钙去除任务上的修复精度和狭窄估计方面,显著优于从头开始训练的模型。尤其是在少样本学习场景下,提升效果更为明显,验证了自监督学习策略的有效性。
🎯 应用场景
该研究成果可应用于临床CTA图像的预处理,提高图像质量,辅助医生更准确地诊断冠状动脉狭窄。通过减少对大量标注数据的依赖,降低了模型训练的成本,加速了深度学习技术在医学影像领域的应用。未来,该方法可以推广到其他医学影像模态和疾病的诊断中。
📄 摘要(原文)
Coronary calcification creates blooming artifacts in Computed Tomography Angiography (CTA), severely hampering the diagnosis of lumen stenosis. While Deep Convolutional Neural Networks (DCNNs) like Dense-Unet have shown promise in removing these artifacts via inpainting, they often require large labeled datasets which are scarce in the medical domain. Inspired by recent advancements in Masked Autoencoders (MAE) for 3D point clouds, we propose \textbf{Dense-MAE}, a novel self-supervised learning framework for volumetric medical data. We introduce a pre-training strategy that randomly masks 3D patches of the vessel lumen and trains the Dense-Unet to reconstruct the missing geometry. This forces the encoder to learn high-level latent features of arterial topology without human annotation. Experimental results on clinical CTA datasets demonstrate that initializing the Calcium Removal network with our MAE-based weights significantly improves inpainting accuracy and stenosis estimation compared to training from scratch, specifically in few-shot scenarios.