A Scalable Distributed Framework for Multimodal GigaVoxel Image Registration
作者: Rohit Jena, Vedant Zope, Pratik Chaudhari, James C. Gee
分类: cs.CV, cs.DC
发布日期: 2025-09-29
💡 一句话要点
提出FFDP框架,实现前所未有的十亿体素多模态图像配准
🎯 匹配领域: 支柱九:具身大模型 (Embodied Foundation Models)
关键词: 图像配准 多模态图像 十亿体素 分布式计算 高性能计算 生物医学图像 深度学习 非GEMM优化
📋 核心要点
- 现有图像配准算法无法有效处理生物医学领域日益增长的超大规模图像数据,成为研究瓶颈。
- FFDP框架通过优化非GEMM操作和实现卷积感知的张量分片,提升了大规模图像配准的效率和可扩展性。
- 实验表明,FFDP显著加速了图像配准流程,降低了内存消耗,并在单GPU上处理更大规模的问题。
📝 摘要(中文)
本文提出FFDP,一个IO感知的非GEMM融合核集合,并结合分布式框架,用于实现前所未有规模的图像配准。图像配准是生物医学和生命科学中一个基础的逆问题,但算法的扩展速度并未跟上图像采集能力的发展。我们的框架通过优化非GEMM瓶颈和实现卷积感知的张量分片,补充了现有的大规模Transformer训练模型并行技术。我们展示了前所未有的能力,仅使用8个A6000 GPU,在大约一分钟内完成了一个100微米离体人脑MRI体素数据的多模态配准,这是一个比标准临床数据大570倍以上的逆问题。FFDP将现有最先进的优化和深度学习配准流程加速高达6-7倍,同时降低峰值内存消耗20-59%。在250微米数据集上的对比分析表明,FFDP可以在单个GPU上拟合比现有SOTA大64倍的问题,并突出了FFDP相对于SOTA图像配准方法的性能和效率优势。
🔬 方法详解
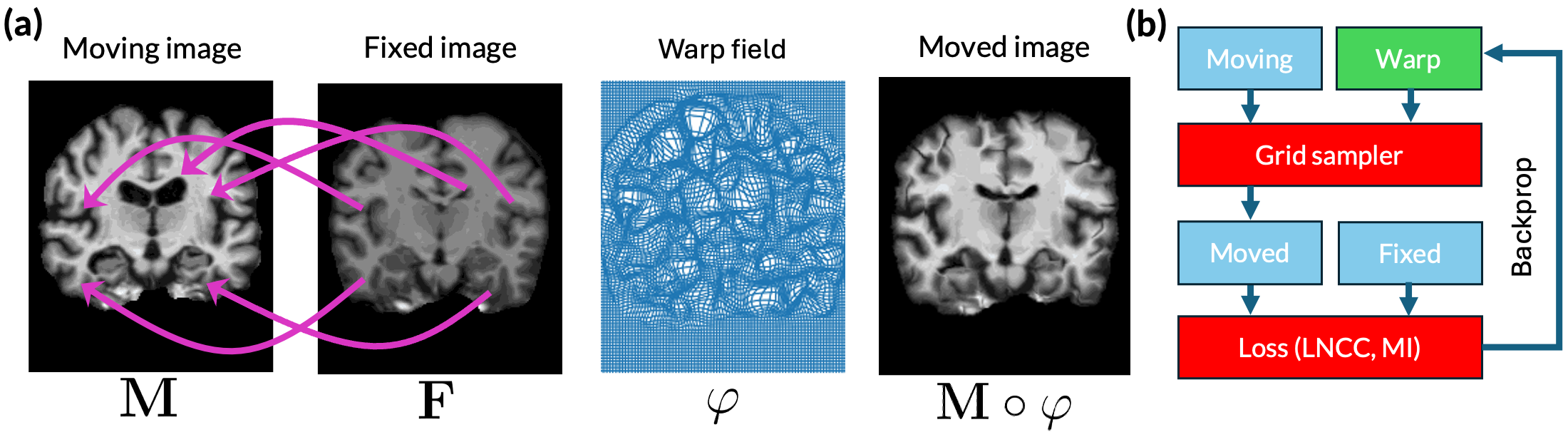
问题定义:论文旨在解决超大规模(GigaVoxel级别)多模态医学图像配准问题。现有方法在处理如此大规模的数据时,面临计算量巨大、内存消耗高、扩展性差等问题,难以满足实际应用需求。尤其是在生物医学领域,高分辨率图像的配准对于疾病诊断和治疗至关重要。
核心思路:论文的核心思路是通过优化IO操作和非GEMM计算,并结合分布式计算框架,来提升大规模图像配准的效率和可扩展性。通过针对性地优化计算瓶颈,减少数据传输,以及利用多GPU并行计算,从而实现对超大规模图像的快速配准。
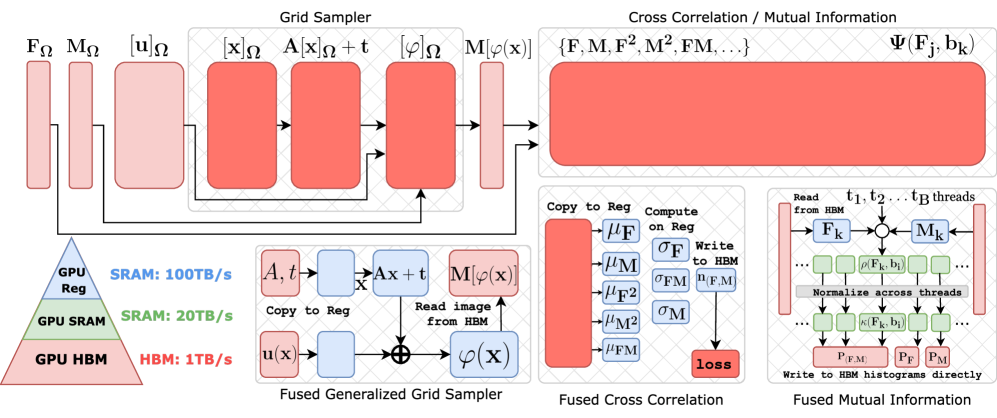
技术框架:FFDP框架包含以下几个主要组成部分:1) IO感知的非GEMM融合核:针对图像配准中的非GEMM计算(如卷积、池化等)进行优化,减少IO开销。2) 分布式框架:利用多GPU进行并行计算,实现张量分片和数据并行。3) 卷积感知的张量分片:根据卷积操作的特性,对张量进行合理分片,减少通信开销。整体流程包括数据加载、预处理、特征提取、配准优化和结果评估等步骤。
关键创新:FFDP的关键创新在于其针对图像配准任务的特点,对非GEMM计算进行了优化,并设计了卷积感知的张量分片策略。这与传统的大规模Transformer训练模型并行技术有所不同,后者主要关注GEMM计算的优化。FFDP更关注图像配准中的IO瓶颈和非线性操作,从而实现了更高的效率。
关键设计:论文中可能涉及的关键设计包括:1) 非GEMM融合核的具体实现方式,例如如何将多个操作融合为一个kernel,减少IO开销。2) 张量分片的策略,例如如何根据卷积核的大小和步长,选择合适的分片方式。3) 分布式计算框架的具体实现,例如如何进行数据同步和通信。4) 配准优化算法的选择和参数设置,例如使用哪种优化器,学习率如何设置等(具体细节未知)。
🖼️ 关键图片

📊 实验亮点
FFDP框架在100微米离体人脑MRI体素数据上实现了前所未有的配准,速度比现有方法快6-7倍,内存消耗降低20-59%。在250微米数据集上,FFDP可以在单个GPU上处理比现有SOTA大64倍的问题。这些结果表明,FFDP在性能和效率方面都具有显著优势。
🎯 应用场景
该研究成果可广泛应用于生物医学图像分析领域,例如脑部疾病研究、肿瘤检测、手术导航等。通过实现对超大规模医学图像的快速精确配准,可以帮助医生更准确地诊断疾病、制定治疗方案,并提高手术的精确性和安全性。未来,该技术有望推动精准医疗的发展,为患者提供更个性化的治疗方案。
📄 摘要(原文)
In this work, we propose FFDP, a set of IO-aware non-GEMM fused kernels supplemented with a distributed framework for image registration at unprecedented scales. Image registration is an inverse problem fundamental to biomedical and life sciences, but algorithms have not scaled in tandem with image acquisition capabilities. Our framework complements existing model parallelism techniques proposed for large-scale transformer training by optimizing non-GEMM bottlenecks and enabling convolution-aware tensor sharding. We demonstrate unprecedented capabilities by performing multimodal registration of a 100 micron ex-vivo human brain MRI volume at native resolution - an inverse problem more than 570x larger than a standard clinical datum in about a minute using only 8 A6000 GPUs. FFDP accelerates existing state-of-the-art optimization and deep learning registration pipelines by upto 6 - 7x while reducing peak memory consumption by 20 - 59%. Comparative analysis on a 250 micron dataset shows that FFDP can fit upto 64x larger problems than existing SOTA on a single GPU, and highlights both the performance and efficiency gains of FFDP compared to SOTA image registration methods.