Can Foundation Models Really Segment Tumors? A Benchmarking Odyssey in Lung CT Imaging
作者: Elena Mulero Ayllón, Massimiliano Mantegna, Linlin Shen, Paolo Soda, Valerio Guarrasi, Matteo Tortora
分类: eess.IV, cs.CV
发布日期: 2025-05-02
💡 一句话要点
基石模型能否有效分割肿瘤?肺部CT影像分割的基准测试
🎯 匹配领域: 支柱九:具身大模型 (Embodied Foundation Models)
关键词: 肺肿瘤分割 基石模型 深度学习 医学影像分析 少样本学习
📋 核心要点
- 肺部肿瘤分割对诊断和治疗至关重要,但肿瘤形态复杂性给自动分割带来挑战。
- 论文探索了基石模型在肺部肿瘤分割中的应用,并与传统模型进行了对比。
- 实验结果表明,基石模型,特别是MedSAM~2,在准确性和效率上优于传统模型。
📝 摘要(中文)
精确的肺肿瘤分割对于改善肿瘤诊断、治疗计划和患者预后至关重要。然而,肿瘤形态、大小和位置的复杂性给自动分割带来了重大挑战。本研究对基于深度学习的分割模型进行了全面的基准分析,比较了U-Net和DeepLabV3等传统架构、nnUNet等自配置模型以及MedSAM和MedSAM~2等基石模型。通过评估两个肺肿瘤分割数据集上的性能,我们评估了各种学习范式(包括少样本学习和微调)下的分割精度和计算效率。结果表明,虽然传统模型在肿瘤勾画方面表现不佳,但基石模型,特别是MedSAM~2,在准确性和计算效率方面均优于它们。这些发现强调了基石模型在肺肿瘤分割方面的潜力,突出了它们在改善临床工作流程和患者预后方面的适用性。
🔬 方法详解
问题定义:论文旨在解决肺部CT影像中肿瘤的精确分割问题。现有方法,如传统的U-Net和DeepLabV3等模型,在处理肿瘤形态、大小和位置的多样性时表现不佳,难以实现准确的肿瘤勾画。此外,训练这些模型通常需要大量的标注数据,成本较高。
核心思路:论文的核心思路是利用预训练的基石模型(Foundation Models),如MedSAM和MedSAM~2,来提升肺部肿瘤分割的性能。基石模型已经在大量数据上进行了预训练,具备较强的泛化能力,可以通过微调或少样本学习的方式快速适应新的分割任务。这种方法可以有效解决传统模型对大量标注数据的依赖问题,并提高分割的准确性和效率。
技术框架:整体框架包括数据预处理、模型选择、训练/微调和性能评估四个主要阶段。首先,对肺部CT影像进行预处理,包括图像标准化、裁剪等操作。然后,选择合适的分割模型,包括传统的U-Net、DeepLabV3、nnUNet以及基石模型MedSAM和MedSAM~2。对于基石模型,可以采用微调或少样本学习的方式进行训练。最后,使用标准的分割指标(如Dice系数、IoU等)评估模型的性能,并比较不同模型之间的差异。
关键创新:论文的关键创新在于将基石模型应用于肺部肿瘤分割任务,并证明了其优越性。与传统的分割模型相比,基石模型具有更强的泛化能力和更高的分割精度。此外,论文还探索了基石模型在少样本学习场景下的性能,进一步降低了对标注数据的需求。
关键设计:论文中,MedSAM和MedSAM~2作为关键的基石模型被使用。具体的技术细节可能包括:使用特定的损失函数(如Dice Loss或Cross-Entropy Loss)进行训练;采用特定的优化器(如Adam或SGD)进行参数更新;调整学习率、batch size等超参数以获得最佳性能。此外,对于MedSAM~2,可能采用了更先进的网络结构或训练策略,以进一步提升分割精度和效率(具体细节未知)。
🖼️ 关键图片

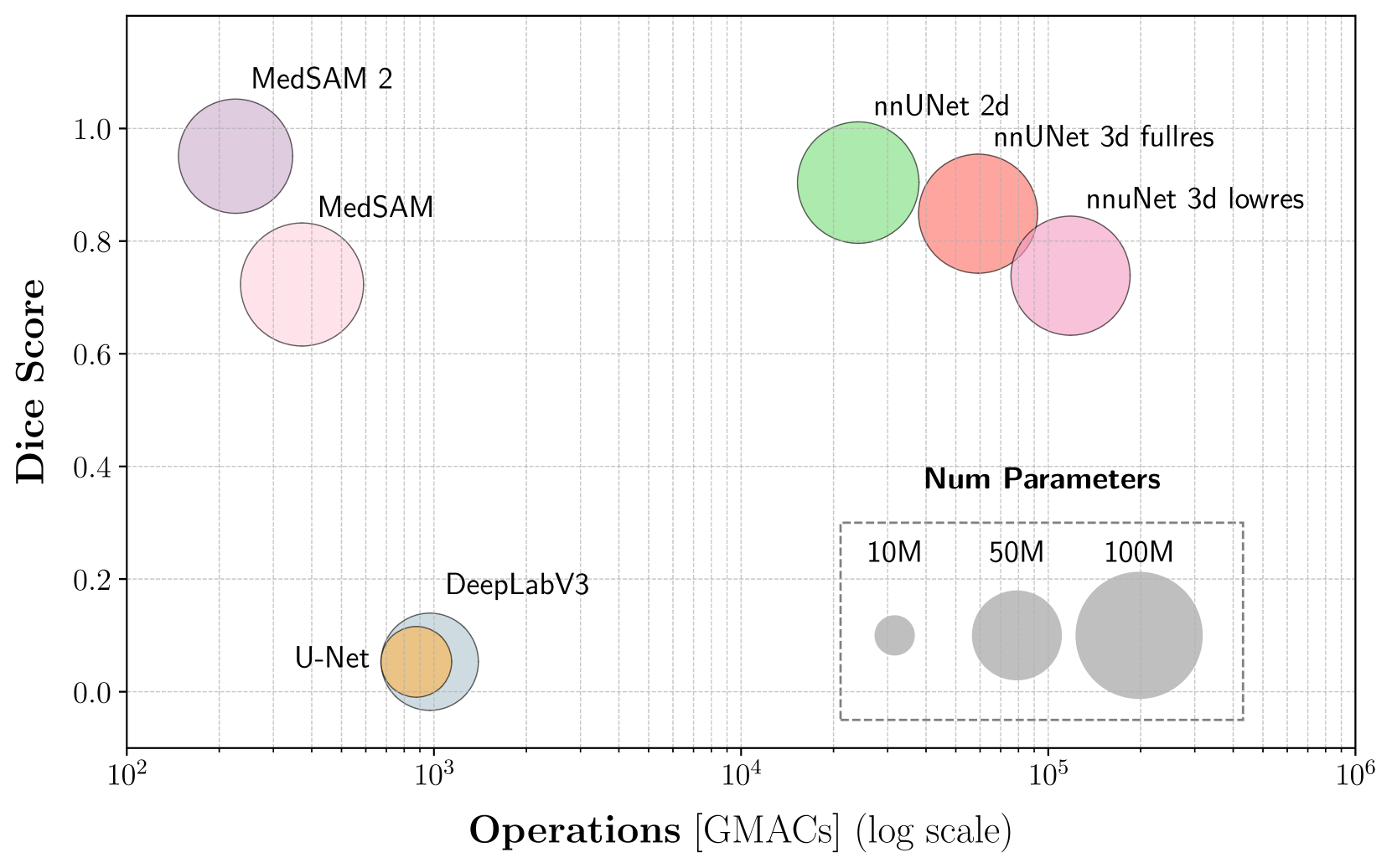
📊 实验亮点
实验结果表明,基石模型MedSAM~2在肺肿瘤分割任务中表现最佳,显著优于传统的U-Net和DeepLabV3等模型。在两个肺肿瘤分割数据集上,MedSAM~2在准确性和计算效率方面均取得了显著提升。尤其是在少样本学习场景下,MedSAM~2仍然能够保持较高的分割精度,展现了其强大的泛化能力。具体的性能数据(如Dice系数、IoU等)在论文中进行了详细的对比和分析(具体数值未知)。
🎯 应用场景
该研究成果可应用于临床辅助诊断、治疗计划制定和疗效评估等领域。精确的肺肿瘤分割可以帮助医生更准确地判断肿瘤的大小、位置和形态,从而制定更有效的治疗方案。此外,该技术还可以用于监测肿瘤的生长和变化,评估治疗效果,并为患者提供个性化的医疗服务。未来,该技术有望集成到医疗影像分析系统中,提高诊断效率和准确性。
📄 摘要(原文)
Accurate lung tumor segmentation is crucial for improving diagnosis, treatment planning, and patient outcomes in oncology. However, the complexity of tumor morphology, size, and location poses significant challenges for automated segmentation. This study presents a comprehensive benchmarking analysis of deep learning-based segmentation models, comparing traditional architectures such as U-Net and DeepLabV3, self-configuring models like nnUNet, and foundation models like MedSAM, and MedSAM~2. Evaluating performance across two lung tumor segmentation datasets, we assess segmentation accuracy and computational efficiency under various learning paradigms, including few-shot learning and fine-tuning. The results reveal that while traditional models struggle with tumor delineation, foundation models, particularly MedSAM~2, outperform them in both accuracy and computational efficiency. These findings underscore the potential of foundation models for lung tumor segmentation, highlighting their applicability in improving clinical workflows and patient outcomes.