UniCoN: Universal Conditional Networks for Multi-Age Embryonic Cartilage Segmentation with Sparsely Annotated Data
作者: Nishchal Sapkota, Yejia Zhang, Zihao Zhao, Maria Gomez, Yuhan Hsi, Jordan A. Wilson, Kazuhiko Kawasaki, Greg Holmes, Meng Wu, Ethylin Wang Jabs, Joan T. Richtsmeier, Susan M. Motch Perrine, Danny Z. Chen
分类: eess.IV, cs.CV
发布日期: 2024-10-16
💡 一句话要点
UniCoN:通用条件网络,用于稀疏标注数据下的多年龄胚胎软骨分割
🎯 匹配领域: 支柱八:物理动画 (Physics-based Animation)
关键词: 胚胎软骨分割 医学图像分析 条件网络 深度学习 多年龄分割 稀疏标注数据 骨软骨发育不良
📋 核心要点
- 现有深度学习软骨分割模型在处理不同年龄段胚胎数据时,准确性和泛化性不足,限制了其在骨软骨发育不良研究中的应用。
- 提出UniCoN,通过引入年龄和空间条件模块,增强模型对软骨形状变化的表征能力,从而提高分割性能和泛化性。
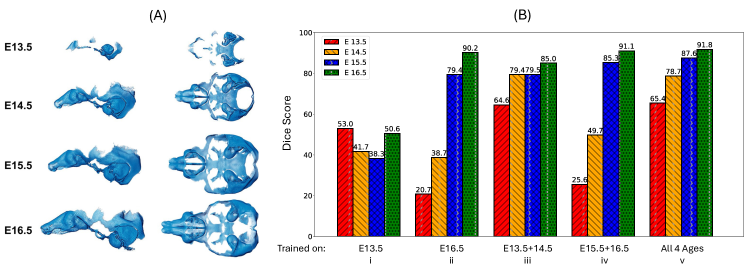
- 实验表明,UniCoN能显著提升多种深度学习架构在多年龄软骨分割任务上的性能,尤其在未见数据上提升显著。
📝 摘要(中文)
骨软骨发育不良影响全球2-3%的新生儿,是一种骨骼和软骨疾病,常导致头部畸形,影响儿童发病率和生活质量。利用小鼠模型研究该疾病面临挑战,需要精确分割胚胎小鼠3D micro-CT图像中的发育软骨。由于手动图像标注负担大、3D micro-CT图像采集成本高昂,以及胚胎软骨形状复杂且快速变化,使用深度学习(DL)方法进行分割非常困难。虽然已经提出了DL方法来自动进行软骨分割,但大多数模型的准确性和泛化性有限,尤其是在来自不同胚胎年龄组的数据中。为了解决这些限制,我们提出了新的DL方法,可以被任何DL架构(包括CNN、Transformer或混合模型)采用,有效地利用年龄和空间信息来提高模型性能。具体来说,我们提出了两种新的机制,一种以离散年龄类别为条件,另一种以连续图像裁剪位置为条件,以实现对跨年龄的软骨形状变化和整个颅骨区域的局部形状细节的准确表示。在多年龄软骨分割数据集上的大量实验表明,将我们的条件模块集成到流行的DL分割架构中时,性能得到了显著且一致的提高。平均而言,我们以最小的计算开销实现了1.7%的Dice分数提升,并在未见过的数据上实现了7.5%的提升。这些结果突出了我们的方法在开发能够处理具有有限标注数据的多样化数据集的鲁棒、通用模型方面的潜力,这是基于DL的医学图像分析中的一个关键挑战。
🔬 方法详解
问题定义:论文旨在解决多年龄胚胎软骨在3D micro-CT图像中的精确分割问题。现有深度学习方法在处理不同年龄段的胚胎数据时,由于软骨形状的快速变化和复杂性,分割精度和泛化能力受到限制,同时,手动标注大量数据成本高昂。
核心思路:论文的核心思路是利用条件网络,将年龄信息和空间位置信息融入到分割模型中,从而使模型能够更好地理解和预测不同年龄段和不同位置的软骨形状。通过条件机制,模型可以学习到软骨形状随年龄变化的规律,以及局部形状的细节信息,从而提高分割的准确性和鲁棒性。
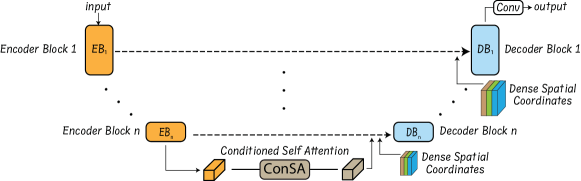
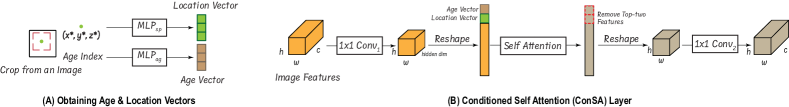
技术框架:UniCoN可以集成到各种深度学习分割架构中,包括CNN、Transformer和混合模型。其主要组成部分包括:1) 年龄条件模块:将离散的年龄类别作为条件输入到网络中,使网络能够区分不同年龄段的软骨形状。2) 空间条件模块:将连续的图像裁剪位置作为条件输入到网络中,使网络能够捕捉局部形状的细节信息。这两个模块可以并行或串行地添加到现有的分割网络中。
关键创新:论文的关键创新在于提出了通用的条件网络UniCoN,能够有效地利用年龄和空间信息来提高多年龄胚胎软骨分割的性能。与现有方法相比,UniCoN不需要针对特定年龄段或特定数据集进行训练,具有更好的泛化能力。此外,UniCoN可以灵活地集成到各种深度学习架构中,具有很强的适应性。
关键设计:年龄条件模块可以使用embedding层将离散的年龄类别转换为连续的向量表示,然后将其与网络的中间特征进行融合。空间条件模块可以使用坐标卷积或类似的方法,将图像裁剪位置的坐标信息编码到特征图中。损失函数可以使用Dice损失或交叉熵损失,并可以根据实际情况进行调整。论文中没有明确给出具体的参数设置,但强调了模块的通用性和易用性。
🖼️ 关键图片
📊 实验亮点
实验结果表明,将UniCoN集成到现有的深度学习分割架构中,可以显著提高多年龄胚胎软骨分割的性能。平均而言,Dice分数提升了1.7%,在未见过的数据上提升了7.5%。这些结果表明,UniCoN具有很强的泛化能力和鲁棒性,能够有效地处理具有有限标注数据的多样化数据集。
🎯 应用场景
该研究成果可应用于骨软骨发育不良等疾病的早期诊断和研究,通过精确分割胚胎软骨,可以更深入地了解疾病的发生发展机制,为开发新的治疗方法提供依据。此外,该方法也可推广到其他医学图像分割任务中,尤其是在处理具有复杂形状变化和有限标注数据的情况下。
📄 摘要(原文)
Osteochondrodysplasia, affecting 2-3% of newborns globally, is a group of bone and cartilage disorders that often result in head malformations, contributing to childhood morbidity and reduced quality of life. Current research on this disease using mouse models faces challenges since it involves accurately segmenting the developing cartilage in 3D micro-CT images of embryonic mice. Tackling this segmentation task with deep learning (DL) methods is laborious due to the big burden of manual image annotation, expensive due to the high acquisition costs of 3D micro-CT images, and difficult due to embryonic cartilage's complex and rapidly changing shapes. While DL approaches have been proposed to automate cartilage segmentation, most such models have limited accuracy and generalizability, especially across data from different embryonic age groups. To address these limitations, we propose novel DL methods that can be adopted by any DL architectures -- including CNNs, Transformers, or hybrid models -- which effectively leverage age and spatial information to enhance model performance. Specifically, we propose two new mechanisms, one conditioned on discrete age categories and the other on continuous image crop locations, to enable an accurate representation of cartilage shape changes across ages and local shape details throughout the cranial region. Extensive experiments on multi-age cartilage segmentation datasets show significant and consistent performance improvements when integrating our conditional modules into popular DL segmentation architectures. On average, we achieve a 1.7% Dice score increase with minimal computational overhead and a 7.5% improvement on unseen data. These results highlight the potential of our approach for developing robust, universal models capable of handling diverse datasets with limited annotated data, a key challenge in DL-based medical image analysis.