Chain-of-Thought Reasoning with Large Language Models for Clinical Alzheimer's Disease Assessment and Diagnosis
作者: Tongze Zhang, Jun-En Ding, Melik Ozolcer, Fang-Ming Hung, Albert Chih-Chieh Yang, Feng Liu, Yi-Rou Ji, Sang Won Bae
分类: cs.CL
发布日期: 2026-02-15
💡 一句话要点
利用大型语言模型和思维链推理进行临床阿尔茨海默病评估与诊断
🎯 匹配领域: 支柱九:具身大模型 (Embodied Foundation Models)
关键词: 阿尔茨海默病诊断 大型语言模型 思维链推理 电子健康记录 临床决策支持
📋 核心要点
- 传统阿尔茨海默病诊断依赖耗时且资源密集的医学影像和临床评估。
- 论文提出利用大型语言模型进行思维链推理,从电子健康记录中提取诊断依据。
- 实验表明,该方法在多个CDR分级任务中显著提升了诊断性能和稳定性。
📝 摘要(中文)
阿尔茨海默病(AD)已成为全球普遍的神经退行性疾病。传统的诊断仍然严重依赖医学影像和医生的临床评估,这在人力专业知识和医疗资源方面通常耗时且资源密集。近年来,大型语言模型(LLM)越来越多地应用于使用电子健康记录(EHR)的医学领域,但它们在阿尔茨海默病评估中的应用仍然有限,特别是因为AD涉及复杂的多因素病因,难以通过影像学方式直接观察。在这项工作中,我们建议利用LLM对患者的临床EHR执行思维链(CoT)推理。与直接在EHR数据上对LLM进行微调以进行AD分类不同,我们的方法利用LLM生成的CoT推理路径为模型提供AD评估的明确诊断原理,然后进行基于CoT的结构化预测。该流程不仅增强了模型诊断内在复杂因素的能力,还提高了不同AD进展阶段预测过程的可解释性。实验结果表明,所提出的基于CoT的诊断框架显著提高了多个CDR分级任务的稳定性和诊断性能,与零样本基线方法相比,F1得分提高了高达15%。
🔬 方法详解
问题定义:阿尔茨海默病的传统诊断方法耗时且依赖专家经验,难以应对日益增长的诊断需求。直接使用大型语言模型进行分类,缺乏可解释性,难以理解模型的诊断依据。现有方法难以有效利用电子健康记录中的复杂信息进行准确评估。
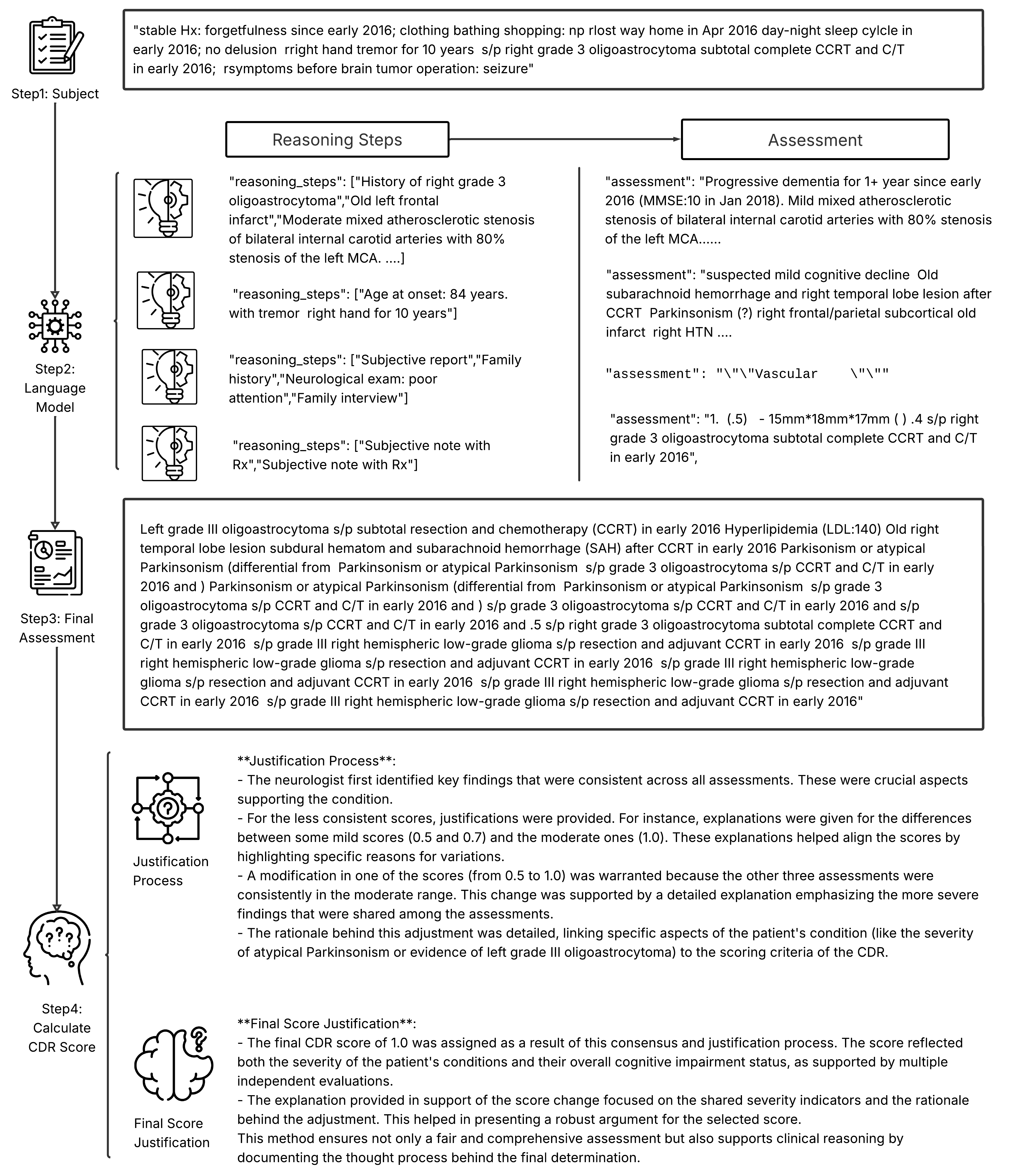
核心思路:论文的核心思路是利用大型语言模型(LLM)的推理能力,模拟医生诊断过程,通过思维链(Chain-of-Thought, CoT)的方式,逐步分析电子健康记录(EHR),生成诊断依据,从而提高诊断的准确性和可解释性。这种方法旨在弥合LLM在复杂医学诊断中应用的差距。
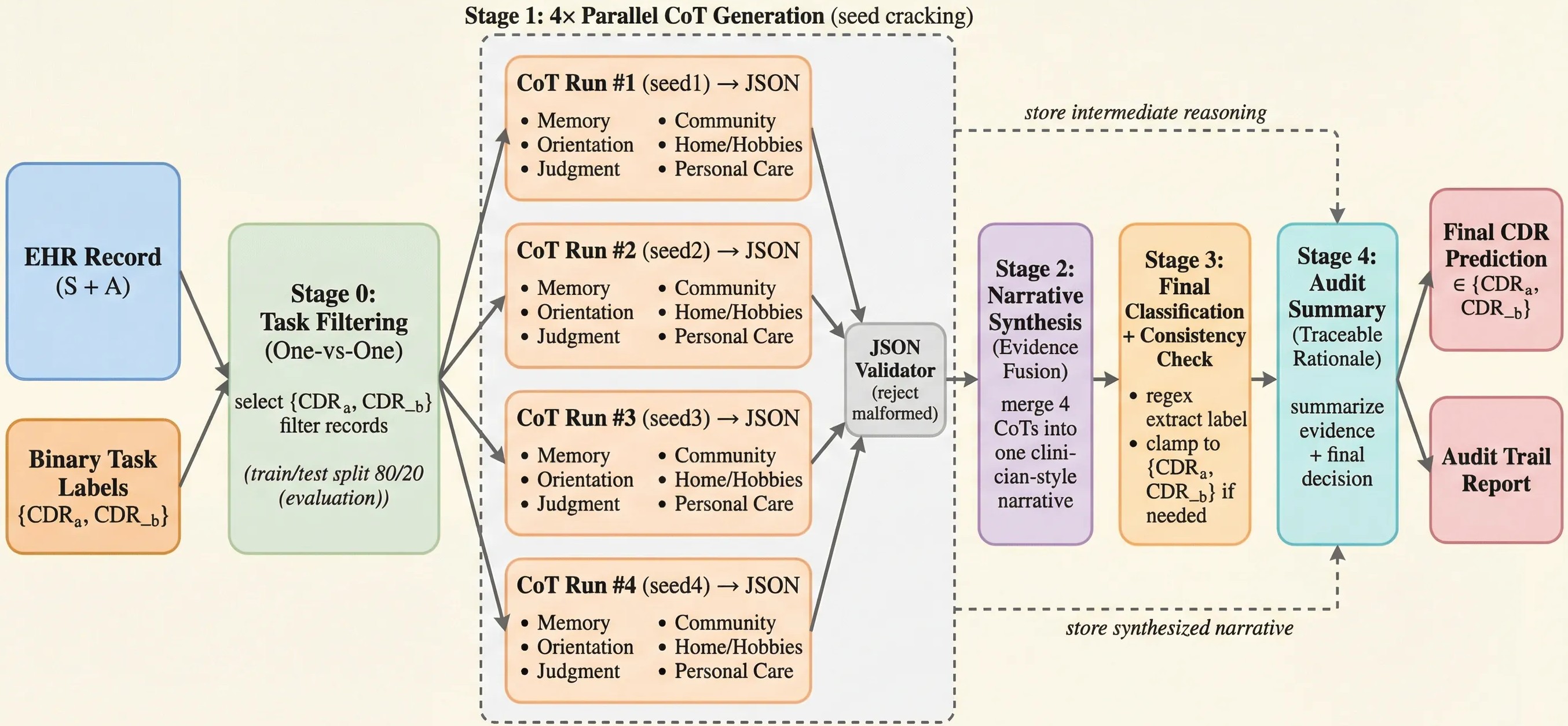
技术框架:该框架主要包含以下几个阶段:1) 输入患者的临床电子健康记录(EHR);2) 使用大型语言模型(LLM)进行思维链(CoT)推理,生成诊断的中间步骤和依据;3) 基于CoT推理的结果,进行结构化的AD评估和预测;4) 输出最终的诊断结果和诊断依据。整个流程旨在模拟医生基于病史和检查结果进行逐步诊断的过程。
关键创新:该方法的核心创新在于将思维链(CoT)推理引入到阿尔茨海默病(AD)的诊断过程中。与直接使用LLM进行分类不同,该方法通过CoT生成诊断依据,提高了模型的可解释性,并使其能够更好地处理复杂的临床信息。此外,该方法避免了对LLM进行直接微调,降低了对大量标注数据的依赖。
关键设计:论文的关键设计包括:1) 如何设计合适的CoT提示(prompt),引导LLM生成有意义的诊断推理过程;2) 如何将CoT推理的结果转化为结构化的AD评估和预测;3) 如何评估CoT推理对诊断性能和可解释性的影响。具体的参数设置、损失函数和网络结构等技术细节在论文中可能没有详细描述,需要进一步查阅原文。
🖼️ 关键图片
📊 实验亮点
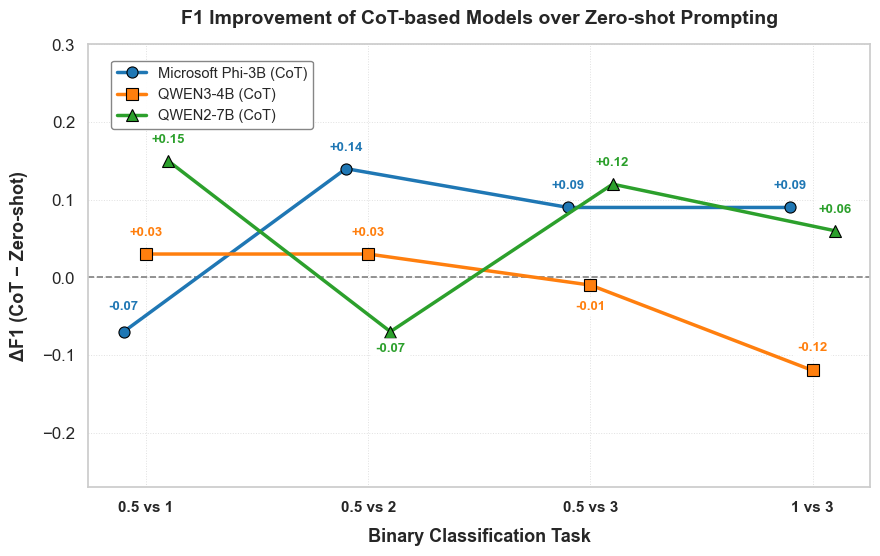
实验结果表明,所提出的基于CoT的诊断框架显著提高了多个CDR分级任务的稳定性和诊断性能,与零样本基线方法相比,F1得分提高了高达15%。这表明CoT推理能够有效提升LLM在复杂医学诊断任务中的表现,并具有实际应用潜力。
🎯 应用场景
该研究成果可应用于临床辅助诊断系统,帮助医生更快速、准确地评估阿尔茨海默病风险,尤其是在医疗资源有限的地区。通过提供可解释的诊断依据,增强医生对AI诊断结果的信任度,促进AI技术在医疗领域的广泛应用。未来可扩展到其他复杂疾病的诊断与评估。
📄 摘要(原文)
Alzheimer's disease (AD) has become a prevalent neurodegenerative disease worldwide. Traditional diagnosis still relies heavily on medical imaging and clinical assessment by physicians, which is often time-consuming and resource-intensive in terms of both human expertise and healthcare resources. In recent years, large language models (LLMs) have been increasingly applied to the medical field using electronic health records (EHRs), yet their application in Alzheimer's disease assessment remains limited, particularly given that AD involves complex multifactorial etiologies that are difficult to observe directly through imaging modalities. In this work, we propose leveraging LLMs to perform Chain-of-Thought (CoT) reasoning on patients' clinical EHRs. Unlike direct fine-tuning of LLMs on EHR data for AD classification, our approach utilizes LLM-generated CoT reasoning paths to provide the model with explicit diagnostic rationale for AD assessment, followed by structured CoT-based predictions. This pipeline not only enhances the model's ability to diagnose intrinsically complex factors but also improves the interpretability of the prediction process across different stages of AD progression. Experimental results demonstrate that the proposed CoT-based diagnostic framework significantly enhances stability and diagnostic performance across multiple CDR grading tasks, achieving up to a 15% improvement in F1 score compared to the zero-shot baseline method.