Multimodal AI predicts clinical outcomes of drug combinations from preclinical data
作者: Yepeng Huang, Xiaorui Su, Varun Ullanat, Intae Moon, Ivy Liang, Lindsay Clegg, Damilola Olabode, Ruthie Johnson, Nicholas Ho, Megan Gibbs, Megan Gibbs, Alexander Gusev, Bino John, Marinka Zitnik
分类: q-bio.QM, cs.AI, cs.LG
发布日期: 2025-03-04 (更新: 2025-09-24)
💡 一句话要点
Madrigal:多模态AI模型,利用临床前数据预测药物组合的临床结果
🎯 匹配领域: 支柱九:具身大模型 (Embodied Foundation Models)
关键词: 多模态学习 药物组合预测 临床结果预测 注意力机制 缺失数据处理
📋 核心要点
- 现有AI模型依赖结构或靶点特征,未能充分利用多模态数据,导致临床预测准确性不足。
- Madrigal模型通过注意力瓶颈模块整合结构、通路、细胞活力和转录组等多模态数据,提升预测能力。
- 实验表明,Madrigal在预测药物不良反应、个性化用药等方面优于现有方法,并与临床试验结果高度吻合。
📝 摘要(中文)
本研究提出了一种名为Madrigal的多模态AI模型,旨在通过临床前数据预测药物组合的临床结果,从而减少后期临床试验失败并加速精准治疗的开发。Madrigal模型融合了结构、通路、细胞活力和转录组数据,用于预测953种临床结果和21842种化合物(包括已批准药物和在研新药)的药物组合效应。该模型采用注意力瓶颈模块统一临床前药物数据的多种模态,并处理训练和推理过程中的数据缺失问题。实验结果表明,Madrigal在预测药物不良反应方面优于单模态方法和现有模型,消融实验验证了模态对齐和多模态的必要性。Madrigal能够捕捉转运蛋白介导的相互作用,并与中性粒细胞减少症、贫血、脱发和低血糖的临床试验差异相符。在2型糖尿病和MASH中,Madrigal支持多重用药决策,并在更安全的候选药物中优先考虑resmetirom。此外,Madrigal还改善了纵向EHR队列和独立肿瘤队列中患者级别的不良事件预测,并预测了原代急性髓系白血病样本和患者来源的异种移植模型中的体外疗效。Madrigal将临床前多模态读数与药物组合的安全性风险联系起来,为更安全的组合设计提供了通用基础。
🔬 方法详解
问题定义:现有AI模型在预测药物组合的临床结果时,主要依赖于药物的结构或靶点信息,忽略了其他重要的生物学信息,如细胞活力、基因表达等。这导致模型无法准确预测药物组合在临床上的真实效果,增加了临床试验失败的风险。此外,临床前数据往往存在缺失,如何有效处理缺失数据也是一个挑战。
核心思路:Madrigal的核心思路是利用多模态学习,将药物的结构、通路、细胞活力和转录组等多维度信息整合起来,从而更全面地了解药物组合的作用机制。通过注意力机制,模型可以自动学习不同模态之间的关联性,并赋予不同模态不同的权重。同时,模型设计了专门的机制来处理缺失数据,保证模型的鲁棒性。
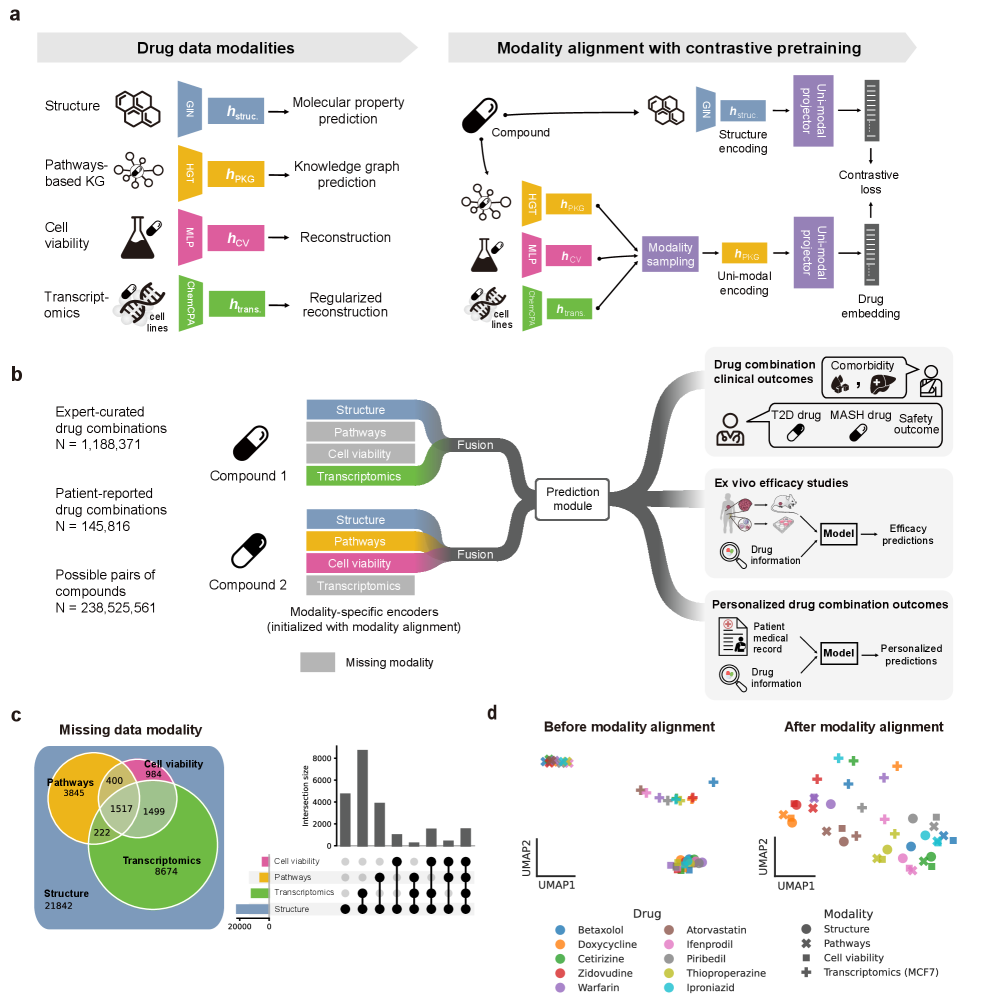
技术框架:Madrigal模型的整体框架包括以下几个主要模块:1) 多模态数据输入模块:负责接收药物的结构、通路、细胞活力和转录组等多模态数据。2) 特征提取模块:对不同模态的数据进行特征提取,例如使用图神经网络提取药物的结构特征,使用基因集富集分析提取通路特征。3) 注意力瓶颈模块:使用注意力机制将不同模态的特征进行融合,并处理缺失数据。4) 预测模块:根据融合后的特征预测药物组合的临床结果。
关键创新:Madrigal最重要的技术创新点在于注意力瓶颈模块。该模块不仅能够有效地融合多模态数据,还能处理数据缺失问题。传统的注意力机制通常需要所有模态的数据都存在,而Madrigal的注意力瓶颈模块可以在某些模态数据缺失的情况下,仍然能够进行有效的特征融合。
关键设计:Madrigal的关键设计包括:1) 使用图神经网络提取药物的结构特征,能够更好地捕捉药物的分子结构信息。2) 使用注意力机制融合多模态特征,能够自动学习不同模态之间的关联性。3) 设计了专门的损失函数来处理数据缺失问题,保证模型的鲁棒性。4) 模型使用了dropout等正则化技术,防止过拟合。
🖼️ 关键图片
📊 实验亮点
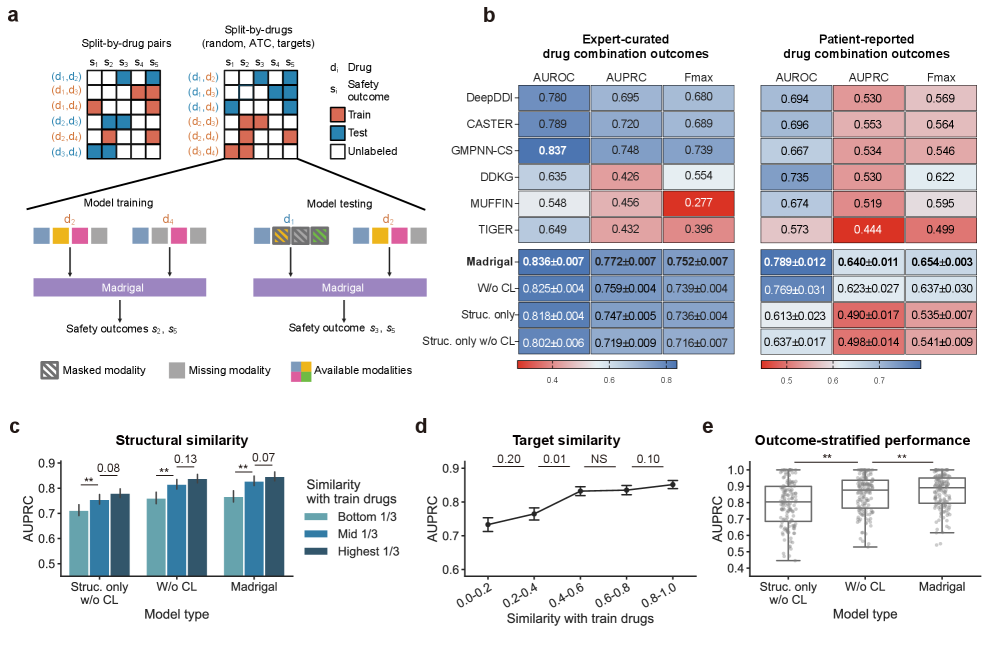
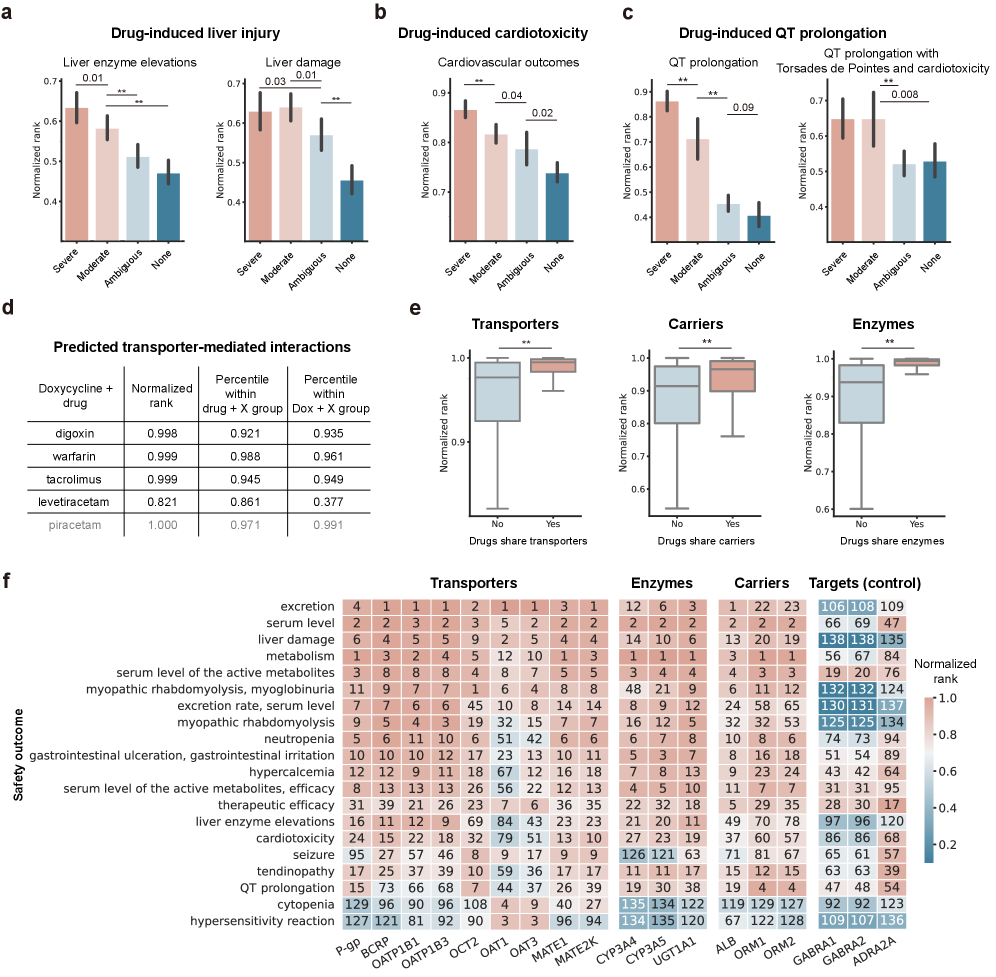
Madrigal在预测药物不良反应方面优于单模态方法和现有模型。例如,在预测药物相互作用方面,Madrigal的性能显著优于DeepDDI等基线模型。此外,Madrigal在个性化用药方面也取得了显著进展,能够根据患者的基因组信息和临床数据,准确预测药物组合的疗效和不良反应。在急性髓系白血病样本和患者来源的异种移植模型中,Madrigal能够预测体外疗效。
🎯 应用场景
Madrigal模型可应用于药物研发的多个阶段,包括早期药物筛选、临床试验设计和个性化用药指导。通过预测药物组合的临床结果,可以减少后期临床试验的失败率,加速新药的开发。此外,Madrigal还可以根据患者的基因组信息和临床数据,预测药物组合的疗效和不良反应,为医生提供个性化的用药建议。该模型有望在肿瘤、糖尿病等复杂疾病的治疗中发挥重要作用。
📄 摘要(原文)
Predicting clinical outcomes from preclinical data is essential for identifying safe and effective drug combinations, reducing late-stage clinical failures, and accelerating the development of precision therapies. Current AI models rely on structural or target-based features but fail to incorporate the multimodal data necessary for accurate, clinically relevant predictions. Here, we introduce Madrigal, a multimodal AI model that learns from structural, pathway, cell viability, and transcriptomic data to predict drug-combination effects across 953 clinical outcomes and 21,842 compounds, including combinations of approved drugs and novel compounds in development. Madrigal uses an attention bottleneck module to unify preclinical drug data modalities while handling missing data during training and inference, a major challenge in multimodal learning. It outperforms single-modality methods and state-of-the-art models in predicting adverse drug interactions, and ablations show both modality alignment and multimodality are necessary. It captures transporter-mediated interactions and aligns with head-to-head clinical trial differences for neutropenia, anemia, alopecia, and hypoglycemia. In type 2 diabetes and MASH, Madrigal supports polypharmacy decisions and prioritizes resmetirom among safer candidates. Extending to personalization, Madrigal improves patient-level adverse-event prediction in a longitudinal EHR cohort and an independent oncology cohort, and predicts ex vivo efficacy in primary acute myeloid leukemia samples and patient-derived xenograft models. Madrigal links preclinical multimodal readouts to safety risks of drug combinations and offers a generalizable foundation for safer combination design.